10.将0.4mol金属Al全部转化为Al(OH)3,消耗a mol HCl、b mol NaOH,则a+b的最小值为( )
| A. | 1.6 | B. | 0.8 | C. | 0.6 | D. | 0.4 |
9.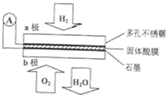 某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法错误的是( )
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法错误的是( )
 某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法错误的是( )
某固体酸燃料电池以CaHSO4固体为电解质传递H+,其基本结构见图,电池总反应可表示为:2H2+O2═2H2O,下列有关说法错误的是( )| A. | 电子通过外电路从a极流向b极 | |
| B. | b极上的电极反应式为:O2+4H++4e-═2H2O | |
| C. | H+由b极通过固体酸电解质传递到a极 | |
| D. | 每转移0.1 mol电子,标准状况下需消耗1.12L的H2 |
7.已知4NH3+5O2═4NO+6H2O,若反应速率分别用υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则正确的是( )
| A. | 4υ(NH3)=5υ(O2) | B. | 5υ(O2)=6υ(H2O) | C. | 2υ(NH3)=3υ(H2O) | D. | 4υ(O2)=5υ(NO) |
6.下列实验的操作和所用的试剂都正确的是( )
| A. | 要鉴别己烯中是否混有少量甲苯,应先加足量溴水,然后再加入酸性高锰酸钾溶液 | |
| B. | 配制浓硫酸和浓硝酸的混酸时,将浓硝酸沿壁缓缓倒入到浓硫酸中 | |
| C. | 制硝基苯时,将盛有混合液的试管直接在酒精灯火焰上加热 | |
| D. | 除去溴苯中少量的溴,可以加水后分液 |
4.针对下面10种元素,完成以下各小题.
(1)常温下,会在浓硫酸中发生钝化的金属是铝(填名称).
(2)化学性质最不活泼的元素是Ne(填元素符号).
(3)镁的原子结构示意图为 .
.
(4)C与N相比,原子半径较小的是N.
(5)最高价氧化物对应的水化物酸性最强的是HClO4碱性最强的是NaOH(填化学式).
(6)常用于制半导体材料的元素是硅.
(7)H2S和HCl相比,热稳定性较强的是HCl.
(8)硫的一种氧化物可使品红溶液褪色,写出该氧化物的化学式SO2,其中硫元素和氧元素的质量比m(S):m(O)=1:1.
(9)常温下金属钠能与水激烈反应,请写出反应的化学方程式:2Na+2H2O=2NaOH+H2↑.
0 169460 169468 169474 169478 169484 169486 169490 169496 169498 169504 169510 169514 169516 169520 169526 169528 169534 169538 169540 169544 169546 169550 169552 169554 169555 169556 169558 169559 169560 169562 169564 169568 169570 169574 169576 169580 169586 169588 169594 169598 169600 169604 169610 169616 169618 169624 169628 169630 169636 169640 169646 169654 203614
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)化学性质最不活泼的元素是Ne(填元素符号).
(3)镁的原子结构示意图为
 .
.(4)C与N相比,原子半径较小的是N.
(5)最高价氧化物对应的水化物酸性最强的是HClO4碱性最强的是NaOH(填化学式).
(6)常用于制半导体材料的元素是硅.
(7)H2S和HCl相比,热稳定性较强的是HCl.
(8)硫的一种氧化物可使品红溶液褪色,写出该氧化物的化学式SO2,其中硫元素和氧元素的质量比m(S):m(O)=1:1.
(9)常温下金属钠能与水激烈反应,请写出反应的化学方程式:2Na+2H2O=2NaOH+H2↑.
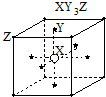
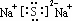 .
.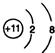 ;
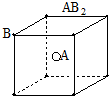
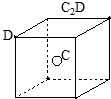
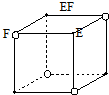
; ;仅由极性键形成的非极性分子的结构式为
;仅由极性键形成的非极性分子的结构式为 ,该分子中心原子的杂化轨道类型是sp3杂化;简单氢化物的沸点最高的是H2O.
,该分子中心原子的杂化轨道类型是sp3杂化;简单氢化物的沸点最高的是H2O.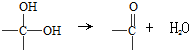
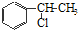 、
、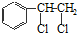 等都是A和Cl2发生反应生成的产物,E是一种发生加聚反应的聚合物物,透光性能好,常用作一些灯饰外壳.过程中一些小分子都已经略去
等都是A和Cl2发生反应生成的产物,E是一种发生加聚反应的聚合物物,透光性能好,常用作一些灯饰外壳.过程中一些小分子都已经略去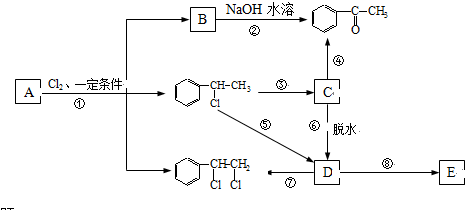
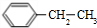 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$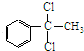 +2HCl,该反应类型为取代反应;
+2HCl,该反应类型为取代反应;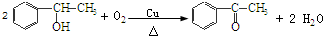 ,该反应类型为氧化反应;
,该反应类型为氧化反应;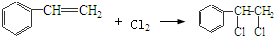 ,该反应类型为加成反应;
,该反应类型为加成反应;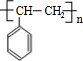 ;
;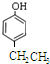 、
、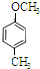 、
、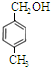 .
.