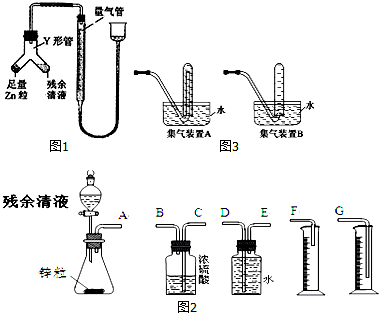
17.某物质的实验式为PtCl4•2NH3,其水溶液不导电,加入AgNO3溶液也不产生沉淀,用强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( )
| A. | 配合物中心原子的电荷数和配位数均为6 | |
| B. | 该配合物可能是平面正方形结构 | |
| C. | Cl-和NH3分子均参与配位 | |
| D. | Cl-没有孤对电子,NH3有孤对电子 |
16.下列分子中的中心原子杂化轨道的类型相同的是( )
| A. | SO3与HCHO | B. | BF3与NH3 | C. | BeCl2与SCl2 | D. | H2O与SO2 |
15.根据下表给出的几种物质的熔、沸点数据判断下列说法中错误的是( )
| 晶体 | NaCl | MgO | AlBr3 | SiCl4 | 共价化合物R |
| 熔点(℃) | 801 | 2852 | 97.5 | -70 | 1723 |
| 沸点(℃) | 1413 | 3600 | 263.3 | 57 | 2230 |
| A. | SiCl4是分子晶体 | B. | MgO比NaCl的晶格能大 | ||
| C. | R是原子晶体 | D. | AlBr3为离子晶体 |
14.化学反应A2+B2=2AB的能量变化如图所示.下列说法正确的是( )


| A. | 该反应是吸热反应 | |
| B. | 生成2molAB需要吸收热量y-x kJ | |
| C. | 断裂1molA-A键和1molB-B键可放出xkJ能量 | |
| D. | 断裂2molA-B键需要吸收ykJ能量 |
13.下列说法中错误的是( )
| A. | 燃料的燃烧反应都是放热反应 | |
| B. | 一定量的燃料完全燃烧放出的热量比不完全燃烧放出的热量大 | |
| C. | 加热后才能发生的化学反应是吸热反应 | |
| D. | 放热反应的逆反应一定是吸热反应 |
11.下表是元素周期表的一部分,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为 .
.
(2)表中能形成两性氢氧化物的元素是铝(填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O═2KAlO2+3H2↑.
(3)①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4(用化学式表示).
(4)③元素与⑩元素两者核电荷数之差是26.
(5)请写出②的氢化物发生催化氧化的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(6)请写出⑤元素的最高价氧化物的水化物与⑦元素的最高价氧化物的水化物反应的离子方程式Al(OH)3+3H+═Al3++3H2O.
0 169434 169442 169448 169452 169458 169460 169464 169470 169472 169478 169484 169488 169490 169494 169500 169502 169508 169512 169514 169518 169520 169524 169526 169528 169529 169530 169532 169533 169534 169536 169538 169542 169544 169548 169550 169554 169560 169562 169568 169572 169574 169578 169584 169590 169592 169598 169602 169604 169610 169614 169620 169628 203614
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)表中能形成两性氢氧化物的元素是铝(填元素名称),写出该元素的单质与⑨最高价氧化物的水化物反应的化学方程式2Al+2KOH+2H2O═2KAlO2+3H2↑.
(3)①、④、⑤、⑥、⑦、⑨六种元素的最高价氧化物的水化物中,按碱性减弱酸性增强的顺序排列为KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4(用化学式表示).
(4)③元素与⑩元素两者核电荷数之差是26.
(5)请写出②的氢化物发生催化氧化的化学方程式4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O.
(6)请写出⑤元素的最高价氧化物的水化物与⑦元素的最高价氧化物的水化物反应的离子方程式Al(OH)3+3H+═Al3++3H2O.

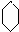
 .反应⑥的化学方程式是
.反应⑥的化学方程式是 .
. 如图为实验室制取氯气的装置图,请根据该图回答下列问题.
如图为实验室制取氯气的装置图,请根据该图回答下列问题.