1.下列化合物属于离子化合物的是( )
| A. | CO2 | B. | CH4 | C. | NH4NO3 | D. | HCl |
20.已知25℃、101kPa条件下,H2、CO、CH4的燃烧分别为286kJ•mol-1、283kJ•mol-1、890kJ•mol-1,若将a mol H2、CO、CH4的混合气体完全燃烧,生成气态CO2和液态H2O,且n(CO2)=n(H2O),则放出的热量(Q)可能为( )
| A. | 284.5a kJ | B. | 586.5a kJ | C. | 555a kJ | D. | 598a kJ |
15.化学与生活密切相关,下列有关说法正确的是( )
| A. | 煤经气化和液化两个物理变化过程,可变为清洁能源 | |
| B. | 维生素C具有还原性,在人体内起抗氧化作用 | |
| C. | 苯酚有一定毒性,不能作消毒剂和防腐剂 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
14.已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
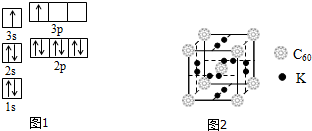
(1)某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)ACl2分子中A的杂化类型为sp杂化.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确不正确(填“正确”或“不正确”),并阐述作出判断的理由:C60是分子晶体,熔化时不需破坏化学键.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4S1,该物质中K原子和C60分子的个数比为3:1.
(5)C、Si、N原子电负性由大到小的顺序是N>C>Si,NCl3分子的VSEPR模型为正四面体.
0 169395 169403 169409 169413 169419 169421 169425 169431 169433 169439 169445 169449 169451 169455 169461 169463 169469 169473 169475 169479 169481 169485 169487 169489 169490 169491 169493 169494 169495 169497 169499 169503 169505 169509 169511 169515 169521 169523 169529 169533 169535 169539 169545 169551 169553 169559 169563 169565 169571 169575 169581 169589 203614
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |

(2)ACl2分子中A的杂化类型为sp杂化.
(3)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.已知金刚石中的C-C的键长为154.45pm,C60中C-C键长为145-140pm,有同学据此认为C60的熔点高于金刚石,你认为此观点是否正确不正确(填“正确”或“不正确”),并阐述作出判断的理由:C60是分子晶体,熔化时不需破坏化学键.
(4)科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.写出基态钾原子的价电子排布式4S1,该物质中K原子和C60分子的个数比为3:1.
(5)C、Si、N原子电负性由大到小的顺序是N>C>Si,NCl3分子的VSEPR模型为正四面体.