题目内容
18.在1L、1mol/L的NaOH溶液中通入16.8L二氧化碳(标况),求溶液中含有NaHCO3和Na2CO3的物质的量.分析 n(CO2)=$\frac{16.8L}{22.4L/mol}$=0.75mol,n(NaOH)=1mol/L×1L=1mol,利用Na、C原子守恒列方程式组进行计算.
解答 解:n(CO2)=$\frac{16.8L}{22.4L/mol}$=0.75mol,n(NaOH)=1mol/L×1L=1mol,设NaHCO3和Na2CO3的物质的量分别是xmol、ymol,利用Na、C原子守恒列方程式组得:
$\left\{\begin{array}{l}{x+2y=1}\\{x+y=0.75}\end{array}\right.$
解得$\left\{\begin{array}{l}{x=0.5}\\{y=0.25}\end{array}\right.$,
答:溶液中含有NaHCO3和Na2CO3的物质的量分别是0.5mol、0.25mol.
点评 本题考查混合物的有关计算,侧重考查分析计算能力,利用原子守恒分析解答即可,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.几种短周期元素的原子半径及主要化合价如下表:
根据以上信息,回答:
(1)写出四种元素的元素名称:X镁 Y铝 Z氮 W氧
(2)写出实验室制取Z的气态氢化物的化学反应方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,常用向下排空气法(方法)来收集Z的气态氢化物.
(3)写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应水化物反应的离子方程式:Al(OH)3+3H+=Al3++3H2O
(4)一定条件下,W单质可以将Z单质从其氢化物中置换出来,请写出其化学反应方程式:4NH3+3O2 $\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +5、+3、-3 | -2 |
(1)写出四种元素的元素名称:X镁 Y铝 Z氮 W氧
(2)写出实验室制取Z的气态氢化物的化学反应方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+CaCl2+2H2O,常用向下排空气法(方法)来收集Z的气态氢化物.
(3)写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应水化物反应的离子方程式:Al(OH)3+3H+=Al3++3H2O
(4)一定条件下,W单质可以将Z单质从其氢化物中置换出来,请写出其化学反应方程式:4NH3+3O2 $\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O.
7.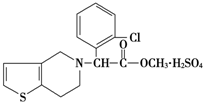 波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
 波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )
波立维是国家刚刚引进的新药,它给中风、心肌梗死等心脏病患者带来福音,波立维属于硫酸氢盐,它的结构如图所示,下列关于它的说法正确的是( )| A. | 该物质的化学式为C16H15ClNO2•H2SO4 | |
| B. | 该物质难溶于水 | |
| C. | 波立维能形成硫酸氢盐是与其结构中的氮原子有关 | |
| D. | 它可以与NaOH溶液反应,1 mol该物质最多可消耗2mol NaOH |
12.两种微粒的质子数和电子数均分别相等,它们不可能是( )
| A. | 两种阳离子 | B. | 一种单质和一种化合物分子 | ||
| C. | 一种分子和一种离子 | D. | 一种原子和一种分子 |
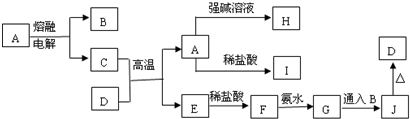
 ,A的结构式为
,A的结构式为 ,A分子的空间构型是三角锥形.
,A分子的空间构型是三角锥形.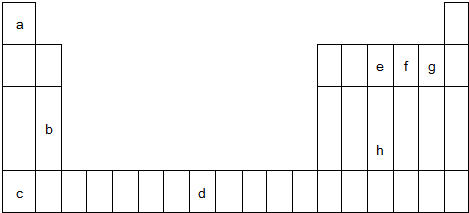
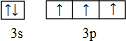 ;
;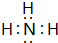 ,其分子的空间构型是三角锥形,分子中e原子的杂化类型是sp3.
,其分子的空间构型是三角锥形,分子中e原子的杂化类型是sp3.