2.I.短周期元素X、Y、Z、W在元素周期表中相对位置如图所示.
其中Y所处的周期序数与族序数相等.按要求回答下列问题:
(1)写出X的原子结构示意图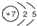 .
.
(2)列举一个事实说明W非金属性强于Z:2HClO4+Na2SiO3=2NaClO4+H2SiO3↓(用化学方程式表示)
II.运用所学化学原理,解决下列问题:
(3)已知:Si+2NaOH+H2O═Na2SiO3+2H2↑.某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为Si-4e-+6OH-=SiO32-+3H2O;
(4)已知:①C(s)+O2(g)═CO2(g)△H=a kJ•mol-1;
②CO2(g)+C(s)═2CO(g)△H=b kJ•mol-1;
③Si(s)+O2(g)═SiO2(s)△H=c kJ•mol-1.
工业上生产粗硅的热化学方程式为2C(s)+SiO2(s)=Si(s)+2CO(g)△H=(a+b-c)kJ•mol-1;
(5)已知:CO(g)+H2O(g) $?_{△}^{催化剂}$ H2(g)+CO2(g).右表为该反应在不同温度时的平衡常数.
则:该反应的△H<0(填“<”或“>”);500℃时进行该反应,且CO和H2O起始浓度相等,CO平衡转化率为75%.
| X | ||||
| Y | Z | W |
(1)写出X的原子结构示意图
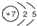 .
.(2)列举一个事实说明W非金属性强于Z:2HClO4+Na2SiO3=2NaClO4+H2SiO3↓(用化学方程式表示)
II.运用所学化学原理,解决下列问题:
(3)已知:Si+2NaOH+H2O═Na2SiO3+2H2↑.某同学利用单质硅和铁为电极材料设计原电池(NaOH为电解质溶液),该原电池负极的电极反应式为Si-4e-+6OH-=SiO32-+3H2O;
(4)已知:①C(s)+O2(g)═CO2(g)△H=a kJ•mol-1;
②CO2(g)+C(s)═2CO(g)△H=b kJ•mol-1;
③Si(s)+O2(g)═SiO2(s)△H=c kJ•mol-1.
工业上生产粗硅的热化学方程式为2C(s)+SiO2(s)=Si(s)+2CO(g)△H=(a+b-c)kJ•mol-1;
(5)已知:CO(g)+H2O(g) $?_{△}^{催化剂}$ H2(g)+CO2(g).右表为该反应在不同温度时的平衡常数.
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
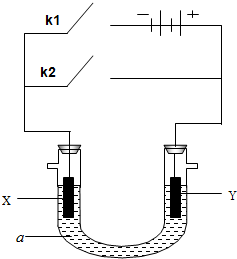
1.某学习小组做了如下实验探究海带中碘元素的存在形式,并测定其中碘元素的含量.
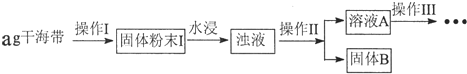
(1)操作Ⅰ为灼烧,则灼烧时应该用坩埚(仪器名称)盛装海带,操作Ⅱ为过滤;
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液.
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性;I2+2S2O32-═2I-+S4O62-将上述溶液稀释配制成200mL溶液,请完成下列实验探究.
限选试剂:3%H2O2溶液、KSCN溶液、FeCl2溶液、稀硫酸
(4)定量检验海带中的碘含量:
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;
②在溶液B加入2滴淀粉溶液,用0.01mol/L Na2S2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,海带中碘元素的百分含量为$\frac{1.27v}{a}%$.假设操作Ⅰ、Ⅱ中碘不损失,原子量I-127)

(1)操作Ⅰ为灼烧,则灼烧时应该用坩埚(仪器名称)盛装海带,操作Ⅱ为过滤;
(2)水浸时通常要将悬浊液煮沸2-3min,目的是加快含碘物质在水中的溶解,以使灰烬中的含碘物质尽可能多的进入溶液.
(3)操作Ⅲ,是同学们对溶液A中碘元素的存在形式进行的探究实验.
[推测]:①以IO3-形式存在; ②以I-形式存在
[查阅资料]:IO3-具有较强的氧化性;I2+2S2O32-═2I-+S4O62-将上述溶液稀释配制成200mL溶液,请完成下列实验探究.
限选试剂:3%H2O2溶液、KSCN溶液、FeCl2溶液、稀硫酸
| 序号 | 实验操作 | 实验现象 | 结论 |
| ① | 取少量稀释后的溶液A加入淀粉后再用硫酸酸化,分装于试管Ⅰ、Ⅱ | 无现象 | |
| ② | 往试管I中加入FeCl2溶液,后加入2滴KSCN溶液并振荡; | 无现象 | 证明不是以IO3-形式存在 |
| ③ | 往试管II中加入3%H2O2溶液并振荡 | 溶液变蓝 | 证明以I-形式存在 |
①取20mL稀释后溶液A分别于锥形瓶,分别用酸式滴定管滴加0.01mol/LKMnO4溶液至溶液刚显浅红色,将I-氧化为I2并得到溶液B;
②在溶液B加入2滴淀粉溶液,用0.01mol/L Na2S2O3溶液,滴定至终点,终点现象为溶液蓝色刚好褪去,30s内不恢复蓝色,记录数据,重复上测定步骤①、②两次,三次平均消耗Na2S2O3溶液体积为VmL,海带中碘元素的百分含量为$\frac{1.27v}{a}%$.假设操作Ⅰ、Ⅱ中碘不损失,原子量I-127)
20.短周期元素W、X、Y、Z在周期表中的位置如图,其中Y所处的周期数与族序数相等.W最外层电子数是其内层电子数的3倍.下列说法不正确的是( )
| … | W | |||
| X | Y | … | Z |
| A. | X、Y、Z、W的原子半径依次减小 | |
| B. | W与X形成的化合物中只含有离子键 | |
| C. | 气态氢化物的稳定性:W>Z | |
| D. | W与Y形成的化合物可分别与NaOH溶液和盐酸反应 |
16.在一定温度下,不能做为反应A2(g)+B2(g)?2AB(g)达到平衡的判断标志是( )
| A. | 单位时间内生成n mol A2的同时消耗n mol A2 | |
| B. | 容器内的各组分的浓度不随时间变化而变化 | |
| C. | 单位时间内生成2n mol AB的同时生成n mol B2 | |
| D. | A2、B2和AB的分子数之比为1:1:2 |
15.下列反应中属于取代反应的是( )
| A. | 乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 苯与氢气在一定条件下反应生成环己烷 | |
| C. | 苯与浓硝酸和浓硫酸的混合液反应生成油状液体 | |
| D. | 乙烯与溴的四氯化碳溶液反应 |
14.将SO2和18O2充入反应容器,当反应达到平衡时,18O原子将( )
0 169269 169277 169283 169287 169293 169295 169299 169305 169307 169313 169319 169323 169325 169329 169335 169337 169343 169347 169349 169353 169355 169359 169361 169363 169364 169365 169367 169368 169369 169371 169373 169377 169379 169383 169385 169389 169395 169397 169403 169407 169409 169413 169419 169425 169427 169433 169437 169439 169445 169449 169455 169463 203614
| A. | 存在于氧气和三氧化硫中 | B. | 只存在于三氧化硫中 | ||
| C. | 三种物质中都有 | D. | 无法判断 |