题目内容
20.短周期元素W、X、Y、Z在周期表中的位置如图,其中Y所处的周期数与族序数相等.W最外层电子数是其内层电子数的3倍.下列说法不正确的是( )| … | W | |||
| X | Y | … | Z |
| A. | X、Y、Z、W的原子半径依次减小 | |
| B. | W与X形成的化合物中只含有离子键 | |
| C. | 气态氢化物的稳定性:W>Z | |
| D. | W与Y形成的化合物可分别与NaOH溶液和盐酸反应 |
分析 短周期元素中,W最外层电子数是其内层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故W为O元素;W、Z同主族,则Z为S元素;Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知X为Na,据此解答.
解答 解:短周期元素中,W最外层电子数是其内层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故W为O元素;W、Z同主族,则Z为S元素;Y所处的周期序数与族序数相等,短周期元素,则Y为第三周期第ⅢA族元素,即Y为Al,由元素的位置可知X为Na.
A.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径X>Y>Z>W,故A正确;
B.W与X形成的化合物有氧化钠、过氧化钠,过氧化钠中含有离子键、共价键,故B错误;
C.非金属性O>S,故氢化物稳定性H2O>H2S,故C正确;
D.W与Y形成的化合物为氧化铝,可分别与NaOH溶液和盐酸反应,故D正确,
故选B.
点评 本题考查位置结构性质的应用,推断元素是解题关键,注意对元素周期律的理解掌握,题目难度不大.

练习册系列答案
相关题目
10.1mol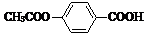 在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
 在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )
在合适条件下与NaOH反应,最多消耗NaOH的物质的量为( )| A. | 2mol | B. | 3 mol | C. | 4 mol | D. | 5 mol |
11.下列制备和收集气体的实验装置合理的是( )
| A. | 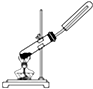 用氯化铵和氢氧化钠固体制NH3 | B. | 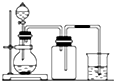 用铜片和稀硝酸制NO | ||
| C. | 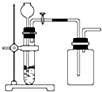 用锌粒和稀硫酸制H2 | D. | 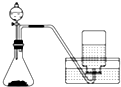 用H2O2和MnO2制O2 |
8.实验室用100mL 1mol•L-1盐酸与锌粉反应制备氢气,下列措施能加快反应速率的是( )
| A. | 改用300mL 1 mol•L-1盐酸 | B. | 降低温度 | ||
| C. | 用锌粒代替锌粉 | D. | 滴加少量CuCl2溶液 |
15.下列反应中属于取代反应的是( )
| A. | 乙烯使酸性高锰酸钾溶液褪色 | |
| B. | 苯与氢气在一定条件下反应生成环己烷 | |
| C. | 苯与浓硝酸和浓硫酸的混合液反应生成油状液体 | |
| D. | 乙烯与溴的四氯化碳溶液反应 |
5.下列有关有机物分离提纯或除杂的方法错误的是( )
| A. | 溴苯中混有溴,加NaOH溶液洗涤、静置、分液 | |
| B. | 除去乙醇中少量乙酸:加入足量生石灰蒸馏 | |
| C. | 乙酸乙酯中有乙酸杂质,可以加入饱和Na2CO3溶液,充分反应后静置分液 | |
| D. | 乙烯中混有SO2,将其通过盛有酸性KMnO4溶液的洗气瓶,再干燥 |
12.利用下列实验装置能完成相应实验的是( )
| A. | 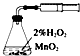 装置测定化学反应速率 | B. | 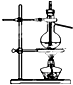 装置模拟海水蒸馏 | ||
| C. | 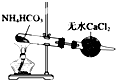 装置制备纯净的NH3 | D. |  装置比较MnO2、Cl2、S的氧化性 |
9.实验室用纯溴和苯在铁离子催化下反应制取溴苯,得到粗溴苯后,要用如下操作精制,正确的操作顺序是
①蒸馏 ②水洗分液 ③用干燥剂干燥 ④10%NaOH溶液洗分液( )
①蒸馏 ②水洗分液 ③用干燥剂干燥 ④10%NaOH溶液洗分液( )
| A. | ①②③④② | B. | ②④②③① | C. | ④②③①② | D. | ②④①②③ |
7.在某温度时,将n mol•L-1氨水滴入10mL 1.0mol•L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

| A. | a点Kw=1.0×10-14 mol2•L-2 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b点:C(NH4+)>C(Cl-)>C(H+)>C(OH-) | |
| D. | 25℃时NH4Cl水解常数为(n-1)×10-7 mol•L-1(用n表示) |