4.CPAE是蜂胶的主要活性成分,由咖啡酸合成CPAE路线如下:
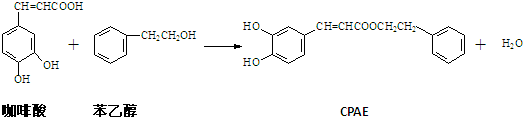
下列分析正确的是( )

下列分析正确的是( )
| A. | 1molCPAE与NaOH溶液,浓溴水和氢气反应时最多消耗的NaOH、Br2和H2的物质的量分别是3mol、4mol和7mol | |
| B. | 咖啡酸分子中至少有9个碳原子共平面 | |
| C. | 咖啡酸、苯乙醇及CPAE都能发生取代,加成和消去反应 | |
| D. | 用FeCl3溶液可以检测上述反应中是否有CPAE生成 |
3.下列说法正确的是( )
| A. | 制取二氧化氮时,用水或NaOH溶液吸收尾气 | |
| B. | 用将Fe(NO3)2样品溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变红的方法来检验Fe(NO3)2晶体是否变质 | |
| C. | 锥形瓶可用作加热的反应器 | |
| D. | 只滴加氨水可以鉴别出NaCl、AlCl3、Na2SO4、MgCl2四种溶液 |
2.化学与生产、生活息息相关,下列说法错误的是( )
0 169125 169133 169139 169143 169149 169151 169155 169161 169163 169169 169175 169179 169181 169185 169191 169193 169199 169203 169205 169209 169211 169215 169217 169219 169220 169221 169223 169224 169225 169227 169229 169233 169235 169239 169241 169245 169251 169253 169259 169263 169265 169269 169275 169281 169283 169289 169293 169295 169301 169305 169311 169319 203614
| A. | 大量燃烧化石燃料是造成雾霾天气的一种重要因素 | |
| B. | 纤维素在人体内可以水解为葡萄糖,故可作人类的营养物质 | |
| C. | 用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+ | |
| D. | “地沟油”禁止食用,但可以用来做肥皂 |
 以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图.回答下列问题:
以甲烷为燃料的新型电池,其成本大大低于以氢为燃料的传统燃料电池,目前得到广泛的研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图.回答下列问题: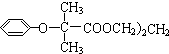
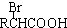 $\stackrel{苯酚钠}{→}$
$\stackrel{苯酚钠}{→}$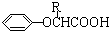
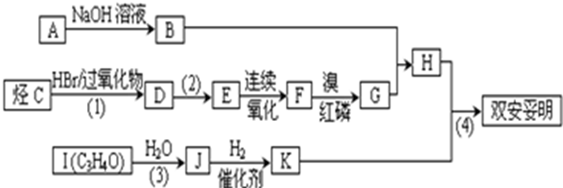

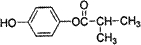 .
.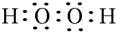 .W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
.W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)