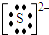
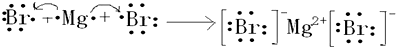
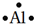3.pH=4的醋酸和pH=4的氯化铵溶液相比,水的电离程度较大的是( )
| A. | 前者 | B. | 后者 | C. | 等于 | D. | 无法确定 |
2.下列关于强、弱电解质的叙述中正确的是( )
| A. | 只有强酸和强碱是强电解质,只有弱酸和弱碱是弱电解质 | |
| B. | 强电解质都是可溶性化合物,弱电解质都是难溶性化合物 | |
| C. | 易溶于水的强电解质水溶液中无溶质分子,易溶的弱电解质水溶液中有溶质分子 | |
| D. | 强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 |
1.下列说法正确的是( )
| A. | 所有自发进行的化学反应都是放热反应 | |
| B. | 放热反应一定比吸热反应的反应速率快 | |
| C. | 由焓判据和熵判据组合而成的复合判据,将更适合于所有的反应过程 | |
| D. | 反应速率快的反应,其反应物的转化率一定高 |
20.将51.2g Cu完全溶于适量浓硝酸中,收集到氮的氧化物(含NO、N2O4、NO2)的混合物共0.8mol,这些气体恰好能被500mL NaOH溶液完全吸收,生成NaNO2和NaNO3两种盐溶液,其中NaNO3的物质的量为0.2mol,则NaOH的浓度为( )(已知:2NO2+2NaOH=NaNO2+NaNO3+H2O、NO+NO2+2NaOH=2NaNO2+H2O)
| A. | 2mol/L | B. | 1.8mol/L | C. | 2.4 mol/L | D. | 3.6 mol/L |
19.下列各组离子中,能大量共存的是( )
| A. | NH4+、Na+、Cl-、OH- | B. | Fe2+、H+、NO3-、SO42- | ||
| C. | NH4+、K+、HCO3-、OH- | D. | Fe3+、NH4+、NO3-、SO42- |
18.元素的性质随着原子序数的递增呈现周期性变化的根本原因是( )
| A. | 元素相对原子质量的递增而引起的变化 | |
| B. | 元素的化合价呈周期性的变化 | |
| C. | 元素原子核外电子排布呈周期性的变化 | |
| D. | 元素的金属性和非金属性呈周期性变化 |
15.在含有FeBr2和FeI2的混合溶液中,通入过量的氯气,然后把溶液加热蒸干、灼烧,最后留下的是( )
①FeCl2②FeCl3③I2④Br2⑤Fe(OH)3⑥Fe2O3⑦FeO.
0 168368 168376 168382 168386 168392 168394 168398 168404 168406 168412 168418 168422 168424 168428 168434 168436 168442 168446 168448 168452 168454 168458 168460 168462 168463 168464 168466 168467 168468 168470 168472 168476 168478 168482 168484 168488 168494 168496 168502 168506 168508 168512 168518 168524 168526 168532 168536 168538 168544 168548 168554 168562 203614
①FeCl2②FeCl3③I2④Br2⑤Fe(OH)3⑥Fe2O3⑦FeO.
| A. | ①③④ | B. | ③⑦ | C. | ③⑤ | D. | ⑥ |
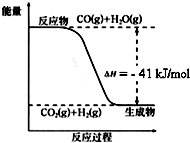 已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.在500℃时的平衡常数 K=9.若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态.
已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.在500℃时的平衡常数 K=9.若在2L的密闭容器中CO和水蒸气的起始浓度都是0.1mol/L,10min时达到平衡状态.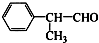 ,工业合成路线如下:
,工业合成路线如下:
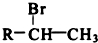
 (R-代表烃基)
(R-代表烃基) 、或
、或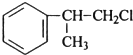 ;
;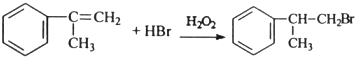 ;
; +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O;
+2H2O;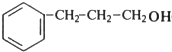 、
、 、
、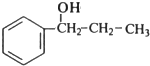 .
.