9.在实验室中常以草酸钠(Na2C2O4)为标准液,通过氧化还原滴定来测定高锰酸钾溶液的浓度,其反应的化学方程式为:C2O42-+MnO4-+H+-→Mn2++CO2↑+H2O.下列有关草酸钠滴定高锰酸钾实验的叙述,正确的是( )
| A. | 滴定过程中,高锰酸钾被氧化,草酸钠被还原 | |
| B. | 用酸式滴定管量取草酸钠溶液 | |
| C. | 该反应中,消耗的草酸钠与高锰酸钾的物质的量之比为5:2 | |
| D. | 为便于滴定终点的判断,滴定时必须往体系中加入指示剂 |
7.下列反应属于吸热反应的是( )
①二氧化碳与赤热的炭反应生成一氧化碳
②液态水汽化
③锌粒与稀H2SO4反应制取H2
④Ba(OH)2•8H2O固体与NH4Cl固体反应
⑤生石灰跟水反应.
①二氧化碳与赤热的炭反应生成一氧化碳
②液态水汽化
③锌粒与稀H2SO4反应制取H2
④Ba(OH)2•8H2O固体与NH4Cl固体反应
⑤生石灰跟水反应.
| A. | ①②④ | B. | ①⑤ | C. | ①③④⑤ | D. | ①④ |
6.如表是元素周期表的一部分(注意:以下各空所涉及的元素填元素符号,不能用字母代替).
(1)写出元素符号:CAl、ECl;
(2)C的离子的结构示意图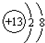 ;
;
(3)用电子式表示AD2的形成过程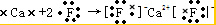 ;
;
(4)A-H八种元素中(填元素符号或化学式)
①原子半径最大的元素是K;单质的氧化性最强的元素是F;
②酸性最强的最高价氧化物对应水化物是HClO4;碱性最强的最高价氧化物对应水化物是KOH.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A |
(2)C的离子的结构示意图
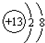 ;
;(3)用电子式表示AD2的形成过程
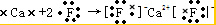 ;
;(4)A-H八种元素中(填元素符号或化学式)
①原子半径最大的元素是K;单质的氧化性最强的元素是F;
②酸性最强的最高价氧化物对应水化物是HClO4;碱性最强的最高价氧化物对应水化物是KOH.
5.下列电子式,正确的是( )
| A. |  | B. | K+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$H]- | ||
| C. |  | D. | 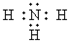 |
4.下列各组元素最高价氧化物对应水化物碱性渐弱,酸性渐强的是( )
| A. | NaOH、Mg(OH)2、H3PO4、H2SO4 | B. | NaOH、KOH、H2SO4、HClO4 | ||
| C. | Be(OH)2、Ca(OH)2、HBrO4、HClO4 | D. | Mg(OH)2、Ba(OH)2、H3PO4、H2SO4 |
1.已知25℃时有关弱电解质的电离平衡常数如表:
根据表中数据回答下列问题:
(1)CH3COO-、CN-、CO32-结合质子(即H+)的能力大小顺序CO32->CN->CH3COO-;25℃时,有等浓度的①CH3COONa溶液、②NaCN溶液、③NaHCO3溶液,三种溶液的pH由大到小的顺序为②>③>① (填序号).
(2)Na2CO3水溶液呈碱性的原因,用离子方程式表示:CO32-+H2O?HCO3-+OH-,溶液中各离子浓度大小顺序:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
(3)NaCN溶液中通入少量二氧化碳,反应的离子方程式为CO2+CN-+H2O=HCN+HCO3-
(4)室温下,向盛一定量的稀氨水烧杯中逐滴加入物质的量浓度相同的醋酸,当恰好中和时,溶液的pH等于7(填“大于”、“等于”或“小于”).
(5)甲、乙两瓶氨水的浓度分别为1mol•L-1、0.1mol•L-1,则c(OH-)甲﹕c(OH-)乙小于10(填“大于”、“等于”或“小于”).
0 168326 168334 168340 168344 168350 168352 168356 168362 168364 168370 168376 168380 168382 168386 168392 168394 168400 168404 168406 168410 168412 168416 168418 168420 168421 168422 168424 168425 168426 168428 168430 168434 168436 168440 168442 168446 168452 168454 168460 168464 168466 168470 168476 168482 168484 168490 168494 168496 168502 168506 168512 168520 203614
| 弱电解质化学式 | CH3COOH | HCN | H2CO3 | NH3.H2O |
| 电离平衡常数 | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7K2=5.6×l0-11 | 1.8×l0-5 |
(1)CH3COO-、CN-、CO32-结合质子(即H+)的能力大小顺序CO32->CN->CH3COO-;25℃时,有等浓度的①CH3COONa溶液、②NaCN溶液、③NaHCO3溶液,三种溶液的pH由大到小的顺序为②>③>① (填序号).
(2)Na2CO3水溶液呈碱性的原因,用离子方程式表示:CO32-+H2O?HCO3-+OH-,溶液中各离子浓度大小顺序:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
(3)NaCN溶液中通入少量二氧化碳,反应的离子方程式为CO2+CN-+H2O=HCN+HCO3-
(4)室温下,向盛一定量的稀氨水烧杯中逐滴加入物质的量浓度相同的醋酸,当恰好中和时,溶液的pH等于7(填“大于”、“等于”或“小于”).
(5)甲、乙两瓶氨水的浓度分别为1mol•L-1、0.1mol•L-1,则c(OH-)甲﹕c(OH-)乙小于10(填“大于”、“等于”或“小于”).



 电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液;X、Y都是惰性电极,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.右图表示一个电解池,装有电解液a,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液;X、Y都是惰性电极,通过导线与直流电源相连.请回答以下问题: 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 盐桥(盛有KNO3琼脂的U型管)构成一个原电池设计的原电池如图所示,盐桥(盛有KNO3琼脂的U型管).请回 答下列问题:
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s) 盐桥(盛有KNO3琼脂的U型管)构成一个原电池设计的原电池如图所示,盐桥(盛有KNO3琼脂的U型管).请回 答下列问题: