10.用眠表示阿伏加德罗常数的值.下列叙述中正确的是( )
| A. | 标准状况下,2.24 LH2O中含有的原子总数为3NA | |
| B. | 等物质的量的Na2O和Na2O2中含有的阴离子总数不同 | |
| C. | Imol甲基(-14C1H3)所含的中子数和电子数分别为8NA、9NA | |
| D. | t℃时,MgCO3的Ksp=4×10-6,则饱和溶液中含Mg2+数目为2×l0-3NA |
9.化学在生产和日常生活中有着重要的应用.下列说法错误的是( )
| A. | 苯、乙醇和乙酸都能发生取代反应 | |
| B. | 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 | |
| C. | 淀粉、油脂、蛋白质都能水解,但水解产物不同 | |
| D. | 白酒中混有少量塑化剂,少量饮用对人体无害,可通过过滤方法除去 |
8.常温下,下列电解质溶液的有关叙述,错误的是( )
| A. | NH4Cl溶液加水稀释后,恢复至原温度,pH和KW均增大 | |
| B. | 在NaHCO3溶液中:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) | |
| C. | pH=4的CH3COOH溶液和pH=4的NH4Cl溶液中,c(H+)相等 | |
| D. | 0.1 mol/L 的NaOH溶液和CH3COOH溶液等体积混合,则c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
7.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 在一定条件下,0.2 mol SO2和0.1 mol O2充分反应,生成SO3的分子数为0.2 NA | |
| B. | 1 L 0.1 mol/L的Na2CO3溶液中阴离子的个数是0.1 NA | |
| C. | 常温常压下,2.24 L 氯气与过量的氢氧化钠溶液完全反应转移的电子数为0.1 NA | |
| D. | 常温常压下,2 g D2O含有的质子数为NA |
6.下列有关描述,正确的是( )
| A. | 苯能使溴水褪色,发生取代反应 | |
| B. | 乙烯使高锰酸钾溶液褪色,发生加成反应 | |
| C. | 乙醇在红热铜丝的作用下,能发生氧化反应 | |
| D. | 葡萄糖在稀硫酸作催化剂,水浴加热条件下可以发生水解反应 |
5.化学与生产、生活、社会密切相关.下列有关说法中正确的是( )
| A. | 航天服材质是由碳化硅、陶瓷和碳纤维等复合而成,它是一种新型有机合成材料 | |
| B. | 煤中含有苯、二甲苯等,可以通过煤的干馏得到,并将它们分离 | |
| C. | 经过一定的化学变化,可以从海水中提取氯化钠、镁、溴等 | |
| D. | 在海轮外壳镶嵌锌块,能减缓轮船的腐蚀,是利用牺牲阳极的阴极保护法 |
4.如图1为元素周期表的一部分,字母下方数值为该元素电负性,根据信息回答下列问题(用相应元素符号进行答题):
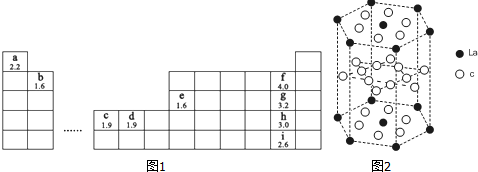
(1)b、h两元素可形成化合物bh2,写出其电子式: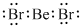 .
.
(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为平面正三角形,eg3、e2g6中心原子e的杂化方式分别为sp2、sp3.
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式:Cu+4HCl=H2CuCl4+H2↑.
(4)f、g、h、i四种元素对应单质分子的键能如下表:
试从原子半径角度阐述f-f键键能反常的原因:F原子半径较小,价电子较多,导致电子云密度增大,极大增加了两原子间的排斥作用,故键能较小,共价键易断裂.
(5)c元素的元素符号是Ni,价电子排布式为3d84s2,下图是一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图2中勾画出该晶体的一个晶胞.计算出该合金的化学式为:LaNi5.

(1)b、h两元素可形成化合物bh2,写出其电子式:
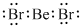 .
.(2)e、g两元素可形成两种化合物eg3、e2g6,eg3的分子构型为平面正三角形,eg3、e2g6中心原子e的杂化方式分别为sp2、sp3.
(3)d元素形成的单质可与g的氢化物浓溶液在加热条件下反应生成一种以二价d离子为内界中心原子(配位数为4)的配位化合物与一种可燃性气体,写出反应的化学方程式:Cu+4HCl=H2CuCl4+H2↑.
(4)f、g、h、i四种元素对应单质分子的键能如下表:
| 共价键 | f-f | g-g | h-h | i-i |
| 键能(kJ/mol) | 157 | 242.7 | 193.7 | 152.7 |
(5)c元素的元素符号是Ni,价电子排布式为3d84s2,下图是一种受到较多关注的c元素单质与金属镧(La)形成的储氢材料的结构示意图,请在图2中勾画出该晶体的一个晶胞.计算出该合金的化学式为:LaNi5.
3.某二元酸H2A在水溶液中以下列方式进行电离:H2A═H++HA-、HA-?H++A2-下列说法正确的是( )
| A. | 室温时,NaHA溶液pH<7,是由于HA-的电离程度大于其水解程度 | |
| B. | 在0.1 mol/L的Na2A溶液中:c(A2-)+c(HA-)+c(H2A)=0.1 mol/L | |
| C. | 在0.1 mol/L的NaHA溶液中,一定有:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) | |
| D. | 向两份等体积NaHA、Na2A的浓度比为1:1的混合溶液中分别加入适当浓度的盐酸与氢氧化钠,其pH随加入酸、碱量的变化图象为: |
2.饱和一元醇R(C5H12O)以银为催化剂进行催化氧化得醛M,再经过酸性KMnO4氧化最终得到羧酸N,则R与N最多可形成酯( )
0 167875 167883 167889 167893 167899 167901 167905 167911 167913 167919 167925 167929 167931 167935 167941 167943 167949 167953 167955 167959 167961 167965 167967 167969 167970 167971 167973 167974 167975 167977 167979 167983 167985 167989 167991 167995 168001 168003 168009 168013 168015 168019 168025 168031 168033 168039 168043 168045 168051 168055 168061 168069 203614
| A. | 9种 | B. | 16种 | C. | 32种 | D. | 64种 |