1.某小组通过实验研究Na2O2与水的反应.
(1)Na2O2与水反应的化学方程式2Na2O2+2H2O=4NaOH+O2↑
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2与酚酞发生了反应.
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂MnO2(填化学式),有气体产生.
Ⅱ.乙同学查阅资料获悉:用KMnO4可以测定H2O2的含量:取15.00mL溶液a,用稀H2SO4酸化,逐滴加入
0.003mol•L-1 KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗20.00mL KMnO4溶液.
①请配平:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
②溶液a中c(H2O2)=0.01mol•L-1.
③溶液褪色速率开始较慢后变快的原因可能是反应生成的Mn2+作催化剂.
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅲ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1mol•L-1 NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色.
Ⅳ.向0.1mol•L-1 NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入O2,溶液颜色无明显变化.
①从实验Ⅲ和Ⅳ中,可得出的结论是碱性条件下,H2O2能与酚酞反应而O2不能.
②同学们进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,加入MnO2,充分反应后,向上层清液中滴入2滴酚酞后变红,10分钟后,溶液颜色无明显变化.
| 操作 | 现象 |
| 向盛有4g Na2O2的烧杯中加入50mL蒸馏水得到溶液a | 剧列反应,产生能使带火星木条复燃的气体 |
| 取5mL溶液a于试管中,滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
(2)ⅱ中溶液褪色可能是溶液a中存在较多的H2O2与酚酞发生了反应.
Ⅰ.甲同学通过实验证实了H2O2的存在:取少量溶液a,加入试剂MnO2(填化学式),有气体产生.
Ⅱ.乙同学查阅资料获悉:用KMnO4可以测定H2O2的含量:取15.00mL溶液a,用稀H2SO4酸化,逐滴加入
0.003mol•L-1 KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至终点时共消耗20.00mL KMnO4溶液.
①请配平:2MnO4-+5H2O2+6H+═2Mn2++5O2↑+8H2O
②溶液a中c(H2O2)=0.01mol•L-1.
③溶液褪色速率开始较慢后变快的原因可能是反应生成的Mn2+作催化剂.
(3)为探究现象ⅱ产生的原因,同学们继续进行了如下实验:
Ⅲ.向H2O2溶液中滴入两滴酚酞,振荡,加入5滴0.1mol•L-1 NaOH溶液,溶液变红又迅速变无色且产生气体,10分钟后溶液变无色.
Ⅳ.向0.1mol•L-1 NaOH溶液中滴入两滴酚酞的,振荡,溶液变红,10分钟后溶液颜色无明显变化;向该溶液中通入O2,溶液颜色无明显变化.
①从实验Ⅲ和Ⅳ中,可得出的结论是碱性条件下,H2O2能与酚酞反应而O2不能.
②同学们进一步通过实验证实了溶液a中滴入酚酞后,H2O2与酚酞发生了化学反应.实验方案是:取少量溶液a于试管中,加入MnO2,充分反应后,向上层清液中滴入2滴酚酞后变红,10分钟后,溶液颜色无明显变化.
20.为了探究AgNO3的热稳定性和氧化性,某化学兴趣小组设计了如下实验.
Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束后,试管中残留固体为黑色Ag.(夹持及加热仪器均省略)
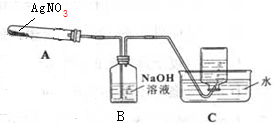
(1)如何检验装置的气密性?连接好仪器后在未加药品之前加热试管,如果C中导气管有气泡冒出,说明气密性良好.
(2)C中集气瓶收集的气体为O2.要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(3)AgNO3分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
(4)甲同学认为仅凭试管A中的红棕色的气体产生就判定NO2产生是错误的,因为无色NO遇到空气也会变成红棕色,所以加热前应当排尽装置中的空气.你是否同甲的观点?并说明理由否,硝酸银分解生成氧气.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,猜测如下:
假设一:Fe被氧化成Fe3+.
假设二:Fe被氧化成Fe2+.
假设三:Fe被氧化成Fe3+或Fe2+.
可选用的试剂:KSCN溶液、酸性KMnO4溶液,氨水,盐酸,硝酸,NaCl溶液
请完成下表:
实验结论:Fe的氧化物为Fe2+和Fe3+.
Ⅰ.AgNO3的热稳定性
利用如图所示的实验装置A加热AgNO3固体,产生红棕色气体,在装置D中收集到无色气体.当反应结束后,试管中残留固体为黑色Ag.(夹持及加热仪器均省略)

(1)如何检验装置的气密性?连接好仪器后在未加药品之前加热试管,如果C中导气管有气泡冒出,说明气密性良好.
(2)C中集气瓶收集的气体为O2.要收集纯净的该气体,正确的操作是等到导气管中气泡均匀放出时再收集.
(3)AgNO3分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
(4)甲同学认为仅凭试管A中的红棕色的气体产生就判定NO2产生是错误的,因为无色NO遇到空气也会变成红棕色,所以加热前应当排尽装置中的空气.你是否同甲的观点?并说明理由否,硝酸银分解生成氧气.
Ⅱ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液的大试管中,一段时间后将铁丝取出.为检验溶液中Fe的氧化产物,猜测如下:
假设一:Fe被氧化成Fe3+.
假设二:Fe被氧化成Fe2+.
假设三:Fe被氧化成Fe3+或Fe2+.
可选用的试剂:KSCN溶液、酸性KMnO4溶液,氨水,盐酸,硝酸,NaCl溶液
请完成下表:
| 操作 | 现象 | 结论或目的 |
| (1)取少量溶液于试管中,向溶液中加入足量NaCl溶液 | - | 除尽Ag+ |
| (2)取少量上述溶液于试管中加入KSCN溶液,振荡 | 溶液变血红色 | 存在Fe3+ |
| (3)取(1)中少量上述溶液于试管中,加入酸性KMnO4溶液,振荡 | 紫色消失 | 存在Fe2+ |
17.从溴乙烷制取1.2-二溴乙烷,下列转化方案中最好的是( )
| A. | CH3CH2Br$\stackrel{NaOH水溶液}{→}$CH3CH2OH$→_{170℃}^{浓H_{2}SO_{4}}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| B. | CH3CH2Br$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| C. | CH3CH2Br$\stackrel{NaOH醇溶液}{→}$CH2=CH2$\stackrel{HBr}{→}$CH2BrCH3$\stackrel{Br_{2}}{→}$CH2BrCH2Br | |
| D. | CH3CH2Br$\stackrel{NaOH醇溶液}{→}$CH2=CH2$\stackrel{Br_{2}}{→}$CH2BrCH2Br |
16.该有机物CH3-CH═CH-Cl能发生( )
①取代反应,②加成反应,③消去反应,④使溴水褪色,⑤使酸性KMnO4溶液褪色,⑥与AgNO3溶液生成白色沉淀,⑦加聚反应.
①取代反应,②加成反应,③消去反应,④使溴水褪色,⑤使酸性KMnO4溶液褪色,⑥与AgNO3溶液生成白色沉淀,⑦加聚反应.
| A. | 以上反应均可发生 | B. | 只有⑦不能发生 | ||
| C. | 只有⑥不能发生 | D. | 只有②不能发生 |
15.某学习小组对Cl2与FeCl2和KSCN混合溶液的反应进行探究.
(1)A中溶液变红的原因是Fe2+被Cl2氧化生成Fe3+,Fe3+与SCN-反应生成红色的,所以溶液变红.
(2)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(3)为探究现象2产生的原因,该小组进行如下实验:
①取A中黄色溶液少许于试管中,加入NaOH溶液,有红褐色沉淀生成,则原溶液中一定存在Fe3+.
②取A中黄色溶液少许于试管中,加入过量的KSCN溶液,最终得到红色溶液.该小组同学此得出结论:产生现象2的原因是SCN-与Cl2发生了反应.
(4)该小组同学猜想SCN-可能被Cl2氧化了,于是又进行了如下探究.
①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是S元素.
②在实验中SCN-中氮元素被氧化为NO3-,检验NO3-存在的方法是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,则证明SCN-中氮元素被氧化为NO3-.
③已知SCN-中各原子均满足8电子稳定结构,试写出SCN-的电子式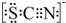 .
.
(5)若SCN-与Cl2反应生成1molCO2,则转移的电子数是16mol.
| 操作 | 现象 |
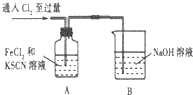 | 1.A中溶液变红 2.稍后,A中溶液由红色变为黄色 |
(2)B中反应的离子方程式是Cl2+2OH-═Cl-+ClO-+H2O.
(3)为探究现象2产生的原因,该小组进行如下实验:
①取A中黄色溶液少许于试管中,加入NaOH溶液,有红褐色沉淀生成,则原溶液中一定存在Fe3+.
②取A中黄色溶液少许于试管中,加入过量的KSCN溶液,最终得到红色溶液.该小组同学此得出结论:产生现象2的原因是SCN-与Cl2发生了反应.
(4)该小组同学猜想SCN-可能被Cl2氧化了,于是又进行了如下探究.
①取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN-中被氧化的元素是S元素.
②在实验中SCN-中氮元素被氧化为NO3-,检验NO3-存在的方法是取足量铜粉于试管中,加入A中黄色溶液和一定量的稀盐酸,加热,观察到试管上方有红棕色气体生成,则证明SCN-中氮元素被氧化为NO3-.
③已知SCN-中各原子均满足8电子稳定结构,试写出SCN-的电子式
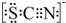 .
.(5)若SCN-与Cl2反应生成1molCO2,则转移的电子数是16mol.
14. 滴定分析是一种操作简便、准确度很高的定量分析方法,它可广泛应用于中和滴定、氧化还原反应等滴定中.某研究性学习小组的同学利用滴定分析法进行下面两项定量分析.
滴定分析是一种操作简便、准确度很高的定量分析方法,它可广泛应用于中和滴定、氧化还原反应等滴定中.某研究性学习小组的同学利用滴定分析法进行下面两项定量分析.
(1)测定NaOH和Na2CO3的混合液中NaOH的含量.实验操作为:先向混合液中加过量的BaCl2溶液使Na2CO3完全转化成BaCO3沉淀,然后用标准盐酸滴定(用酚酞作指示剂).
①向混有BaCO3沉淀的NaOH溶液中直接滴入盐酸,则终点颜色的变化为溶液的颜色由红色变为浅红色,为何此种情况能测出NaOH的含量?能,酚酞的变色在碱性范围内,此时只有NaOH与HCl反应.
②滴定时,若滴定管中的滴定液一直下降到活塞处才达到滴定终点,则能否由此准确地计算出结果?不能,滴定管的下端无刻度,若滴定液一直下降到活塞处,无法测出溶液的体积
(2)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量.准确称取5.0000g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI═3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250mL,然后用5.0×10-4mol•L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+
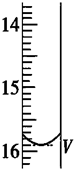
2S2O32-═2I-+S4O62-).取用Na2S2O3标准溶液应该用碱式式滴定管.有关实验数值如表(第一次滴定终点的数据如图所示,请将读得的数据填入表中).
该碘盐中碘元素的百分含量为0.03175%,下列操作中,会导致所测得的碘元素的百分含量偏大的是b.
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水.
 滴定分析是一种操作简便、准确度很高的定量分析方法,它可广泛应用于中和滴定、氧化还原反应等滴定中.某研究性学习小组的同学利用滴定分析法进行下面两项定量分析.
滴定分析是一种操作简便、准确度很高的定量分析方法,它可广泛应用于中和滴定、氧化还原反应等滴定中.某研究性学习小组的同学利用滴定分析法进行下面两项定量分析.(1)测定NaOH和Na2CO3的混合液中NaOH的含量.实验操作为:先向混合液中加过量的BaCl2溶液使Na2CO3完全转化成BaCO3沉淀,然后用标准盐酸滴定(用酚酞作指示剂).
①向混有BaCO3沉淀的NaOH溶液中直接滴入盐酸,则终点颜色的变化为溶液的颜色由红色变为浅红色,为何此种情况能测出NaOH的含量?能,酚酞的变色在碱性范围内,此时只有NaOH与HCl反应.
②滴定时,若滴定管中的滴定液一直下降到活塞处才达到滴定终点,则能否由此准确地计算出结果?不能,滴定管的下端无刻度,若滴定液一直下降到活塞处,无法测出溶液的体积
(2)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量.准确称取5.0000g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI═3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250mL,然后用5.0×10-4mol•L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+
2S2O32-═2I-+S4O62-).取用Na2S2O3标准溶液应该用碱式式滴定管.有关实验数值如表(第一次滴定终点的数据如图所示,请将读得的数据填入表中).
| 滴定次数 | 待测液的体积(mL) | 滴定前的读数(mL) | 滴定后的读数(mL) |
| 第一次 | 25.00 | 0.00 | V=15.90 |
| 第二次 | 25.00 | 0.00 | 14.99 |
| 第三次 | 25.00 | 0.00 | 15.01 |
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水.
12.已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等.某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如图:
下列说法不正确的是( )
0 167834 167842 167848 167852 167858 167860 167864 167870 167872 167878 167884 167888 167890 167894 167900 167902 167908 167912 167914 167918 167920 167924 167926 167928 167929 167930 167932 167933 167934 167936 167938 167942 167944 167948 167950 167954 167960 167962 167968 167972 167974 167978 167984 167990 167992 167998 168002 168004 168010 168014 168020 168028 203614

下列说法不正确的是( )
| A. | 步骤①②的名称分别为溶解、过滤 | |
| B. | 步骤③中使用的化学仪器有酒精灯、三角架、泥三角、坩埚、玻璃棒 | |
| C. | 步骤①②③中都使用了玻璃棒,且三个操作中玻璃棒的作用不完全相同 | |
| D. | 步骤④的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O |

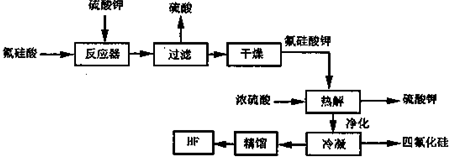
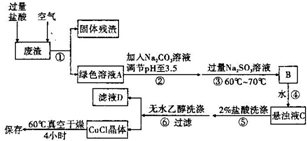 通常情况下,CuCI为白色粉末,微溶于水,不溶于乙醇,常用作有机合成的催化剂,并用于颜料、防腐等工业.CuCI露置于空气中较易被氧化为绿色的高价铜盐,见光易分解,变成褐色,受潮易变成蓝到棕色.有机硅装置在单体合成的生产过程中,副产高沸物、共沸物、硅渣浆液.其中硅渣浆液中含有Si、Cu及有机硅单体等物质,硅渣浆液经过处理后可得到富含硅、铜、碳的废渣.如图是从废渣中制取CuCI的一种工艺流程图.
通常情况下,CuCI为白色粉末,微溶于水,不溶于乙醇,常用作有机合成的催化剂,并用于颜料、防腐等工业.CuCI露置于空气中较易被氧化为绿色的高价铜盐,见光易分解,变成褐色,受潮易变成蓝到棕色.有机硅装置在单体合成的生产过程中,副产高沸物、共沸物、硅渣浆液.其中硅渣浆液中含有Si、Cu及有机硅单体等物质,硅渣浆液经过处理后可得到富含硅、铜、碳的废渣.如图是从废渣中制取CuCI的一种工艺流程图.