��Ŀ����
1��ijС��ͨ��ʵ���о�Na2O2��ˮ�ķ�Ӧ��| ���� | ���� |
| ��ʢ��4g��Na2O2���ձ��м���50mL����ˮ�õ���Һa | ���з�Ӧ��������ʹ������ľ����ȼ������ |
| ȡ5mL��Һa���Թ��У��������η�̪ | ������Һ��� ����10���ֺ���Һ��ɫ���Ա�dz���Ժ���Һ��Ϊ��ɫ |
��2��������Һ��ɫ��������Һa�д��ڽ϶��H2O2���̪�����˷�Ӧ��
��ͬѧͨ��ʵ��֤ʵ��H2O2�Ĵ��ڣ�ȡ������Һa�������Լ�MnO2���ѧʽ���������������
����ͬѧ�������ϻ�Ϥ����KMnO4���ԲⶨH2O2�ĺ�����ȡ15.00mL��Һa����ϡH2SO4�ữ����μ���
0.003mol•L-1��KMnO4��Һ���������壬��Һ��ɫ���ʿ�ʼ�������죬���յ�ʱ������20.00mL��KMnO4��Һ��
������ƽ��2MnO4-+5H2O2+6H+�T2Mn2++5O2��+8H2O
����Һa��c��H2O2��=0.01mol•L-1��
����Һ��ɫ���ʿ�ʼ���������ԭ������Ƿ�Ӧ���ɵ�Mn2+��������
��3��Ϊ̽����������ԭ��ͬѧ�Ǽ�������������ʵ�飺
����H2O2��Һ�е������η�̪��������5��0.1mol•L-1 NaOH��Һ����Һ�����Ѹ�ٱ���ɫ�Ҳ������壬10���Ӻ���Һ����ɫ��
������0.1mol•L-1 NaOH��Һ�е������η�̪�ģ�����Һ��죬10���Ӻ���Һ��ɫ�����Ա仯�������Һ��ͨ��O2����Һ��ɫ�����Ա仯��
�ٴ�ʵ���͢��У��ɵó��Ľ����Ǽ��������£�H2O2�����̪��Ӧ��O2���ܣ�
��ͬѧ�ǽ�һ��ͨ��ʵ��֤ʵ����Һa�е����̪��H2O2���̪�����˻�ѧ��Ӧ��ʵ�鷽���ǣ�ȡ������Һa���Թ��У�����MnO2����ַ�Ӧ�����ϲ���Һ�е���2�η�̪���죬10���Ӻ���Һ��ɫ�����Ա仯��
���� ��1������ʵ�����������ʹ������ľ����ȼ�����壬˵����������������Һ���˵���м����ɣ��ݴ�д��ѧ����ʽ��
��2������ʹH2O2��������ͨ����MnO2���������ݴ˴��⣻
��KMnO4��H2O2��Ӧ�������������˵������������Һ��ɫ˵��KMnO4����ԭ���ٸ��ݵ��ӵ�ʧ�غ�͵���غ��д�����ӷ���ʽ��
�ڸ���KMnO4��H2O2��Ӧ�����ʵ���֮�����H2O2�����ʵ��������������Һa��c��H2O2����
��һ��������ڿ�ʼʱ��Ӧ��Ũ�Ƚϴ�Ӧ����Ӧ���Ͽ죬����������Һ��ɫ���ʿ�ʼ�������죬������Dz����µ����ʣ��Ҵ����ʶԷ�Ӧ�д����ã��Ӷ��ӿ��˷�Ӧ���ʣ��ݴ˷�����
��3���ٷ����Ա�ʵ���͢�����֪�ڢ�����H2O2��Һ������������������������ͬ������������˲��죬˵��������Һ�����Ѹ�ٱ���ɫ����H2O2�������������ݴ˴��⣻
��Ҫ��һ����֤��Һa�е����̪��H2O2���̪�����˻�ѧ��Ӧ�������루3���еĢ��ٶԱȣ��������Ƚ�H2O2�ֽ�����ٿ���ɫ�仯������Ϳ�˵�����⣬�ݴ˴��⣮
��� �⣺��1������ʵ�����������ʹ������ľ����ȼ������˵����������������Һ���˵���м����ɣ��ݴ�д��ѧ����ʽΪ��2Na2O2+2H2O=4NaOH+O2����
�ʴ�Ϊ��2Na2O2+2H2O=4NaOH+O2����
��2������ʹH2O2��������ͨ����MnO2��������
�ʴ�Ϊ��MnO2��
��KMnO4��H2O2��Ӧ�������������˵������������Һ��ɫ˵��KMnO4����ԭ���ٸ��ݵ��ӵ�ʧ�غ�͵���غ��д�����ӷ���ʽΪ��2MnO4-+5H2O2+6H+=2Mn2++5O2��+8H2O��
�ʴ�Ϊ��2��5��6H+��2��5��8��
�ڸ���KMnO4��H2O2��Ӧ�����ӷ���ʽ��֪��ϵʽΪ��
2MnO4-��5H2O2
2mol 5mol
0.003mol•L-1��0.02L n��H2O2��
��n��H2O2��=1.5��10-4mol
��c��H2O2��=$\frac{1.5��1{0}^{-4}mol}{1.5��1{0}^{-2}L}$=0.01mol/L
�ʴ�Ϊ��0.01mol/L��
��һ��������ڿ�ʼʱ��Ӧ��Ũ�Ƚϴ�Ӧ����Ӧ���Ͽ죬����������Һ��ɫ���ʿ�ʼ�������죬������Dz����µ����ʣ��Ҵ����ʶԷ�Ӧ�д����ã��Ӷ��ӿ��˷�Ӧ���ʣ��������ӷ�Ӧ2MnO4-+5H2O2+6H+=2Mn2++5O2��+8H2O����֪��������IJ���ΪMn2+��
�ʴ�Ϊ����Ӧ���ɵ�Mn2+��������
��3���ٷ����Աȷ����Ա�ʵ���͢�����֪�ڢ�����H2O2��Һ������������������������ͬ������������˲��죬��˵��������Һ�����Ѹ�ٱ���ɫ����H2O2������������
�ʴ�Ϊ�����������£�H2O2�����̪��Ӧ��O2���ܣ�
��Ҫ��һ����֤��Һa�е����̪��H2O2���̪�����˻�ѧ��Ӧ�������루3���еĢ��ٶԱȣ��������Ƚ�H2O2�ֽ�����ٿ���ɫ�仯������Ϳ�˵�������ˣ�
�ʴ�Ϊ������MnO2����ַ�Ӧ�����ϲ���Һ�е���2�η�̪���죬10���Ӻ���Һ��ɫ�����Ա仯��
���� ���������ʵ�����Ϊ���������������ӷ���ʽ��д����ѧ���㡢ʵ���������ѧ���ۺ�����Ԫ�ػ�����֪ʶ������Ҫ��ϸߣ��ѶȽϴ�

ͬʱ����SiO2��FeCO3��Fe2O3��A12O3�����ʣ�����Ϊԭ����ȡ����ͭ�Ĺ���
��������ͼ��ʾ��
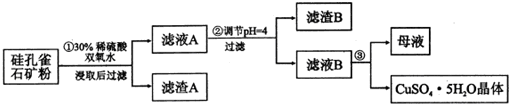
��1������1���ȼ�������ϡ���ᣬ�ټ���˫��ˮ����˫��ˮ����÷�Ӧ�����ӷ���ʽ��2Fe2++H2O2+2H+�T2Fe3++2H2O
��2������ڵ�����ҺpH������ѡ�õ��Լ���BC��������ĸ��ţ�
A��Al2O3B��CuOC��CuCO3•Cu��OH��2
��3���й��������↑ʼ��������ȫ������pH���±���
| �������� | Al��OH��3 | Fe��OH��3 | Fe��OH��2 | Cu��OH��2 |
| ��ʼ������pH | 3.3 | 1.5 | 6.5 | 4.2 |
| ������ȫ��pH | 5.2 | 3.7 | 9.7 | 6.7 |
��4������ҺBͨ������Ũ������ȴ�ᾧ�����˵Ȳ����ɵõ�����ͭ���壮
��5������ͭҲ������ͭ�������ڸ��¡����������»����Ƶã��÷�Ӧ�Ļ�ѧ����ʽ�ǣ�
ȡ384gCuS��һ�������º�������ȫ��Ӧ��������2CuS+3O2=2CuO+2SO2��
4CuS+5O2=2Cu2O+4SO2��������Ӧ�������ù�����Cu��O�����ʵ���֮��n��Cu����n��O��=4��a����ʱ���Ŀ��������ʵ���Ϊb mol����a=a=$\frac{2}{5}$b-8��������ռ���������1/5��
��ȡ����Ӧ���ڼӳɷ�Ӧ������ȥ��Ӧ����ʹ��ˮ��ɫ����ʹ����KMnO4��Һ��ɫ������AgNO3��Һ���ɰ�ɫ�������Ӿ۷�Ӧ��
| A�� | ���Ϸ�Ӧ���ɷ��� | B�� | ֻ�Т߲��ܷ��� | ||
| C�� | ֻ�Т��ܷ��� | D�� | ֻ�Тڲ��ܷ��� |
| A�� | pH��С | B�� | $\frac{c��N{H}_{4}^{+}��}{c��O{H}^{-}��}$���� | ||
| C�� | ˮ�ĵ���̶��ȼ�С������ | D�� | Kb��NH3•H2O������ |
| A�� | ��������� | B�� | �����³ʹ�̬ | ||
| C�� | �������ƽ��ʯ��Ӳ�� | D�� | �ױ����� |