17.下列反应中,反应后固体物质增重的是( )
| A. | 高温灼烧CuO固体 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 硫粉与铁粉混合加热 | D. | 将金属Cu投入FeCl3溶液中 |
16.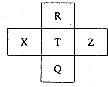 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )
 元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示,R元素原子最外层电子数等于其电子层数的3倍,下列判断正确的是( )| A. | X元素的最高价氧化物对应的水化物酸性强于T元素 | |
| B. | 原子半径:R<T<Z | |
| C. | Z的单质可从T的气态氢化物中置换出T的单质 | |
| D. | R、T、Q最高正价相同 |
15.化学已渗透到人类生活的各个方面,下列说法中不正确的是( )
| A. | BaSO4和BaCO3均难溶于水,均可用作“钡餐” | |
| B. | 轮船的外壳和铁锅等生锈主要发生了电化学腐蚀 | |
| C. | 钻石和水晶都是人们熟知的宝石,但其化学成分不同 | |
| D. | 硫酸铁和明矾都可用于净水 |
14.在A、B、C三支试管中分别加入等体积0.1 mol/L Fe2(SO4)3溶液.将A试管在酒精灯火焰上加热到沸腾,向B试管中加3滴6 mol/L H2SO4.下列说法不正确的是( )
| A. | 最终三支试管的颜色各不相同 | |
| B. | A试管中Fe(OH)3含量最高 | |
| C. | 直接加热蒸发Fe2(SO4)3溶液可得到Fe2(SO4)3晶体 | |
| D. | B试管中Fe2(SO4)3不能发生水解 |
13.以下反应中,Q1>Q2的是( )
| A. | S(s)+O2(g)→SO2(g)+Q1kJ;S(g)+O2(g)→SO2(g)+Q2kJ | |
| B. | H2(g)+$\frac{1}{2}$O2(g)→H2O(l)+Q1kJ;H2(g)+$\frac{1}{2}$O2(g)→H2O(g)+Q2kJ | |
| C. | NaOH(aq)+HCl(aq)→NaCl(aq)+H2O(l)+Q1kJ NaOH(aq)+HAc(aq)→NaAc(aq)+H2O(l)+Q2kJ | |
| D. | H2(g)+Cl2(g)→2HCl(g)+Q1kJ,H2(g)+I2(g)→2HI(g)+Q2kJ |
12.能在水溶液中大量共存的离子组是( )
| A. | H+、Fe3+、ClO-、Cl- | B. | H+、NH4+、Fe2+、NO3- | ||
| C. | Ag+、K+、Cl-、SO42- | D. | K+、AlO2-、Cl-、OH- |
9.短周期主族元素X、Y、Z、W的原子序数依次增大.X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族.下列说法正确的是( )
| A. | 原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X) | |
| B. | Y分别与Z、W形成的化合物中化学键类型相同 | |
| C. | X的最高价氧化物对应水化物的酸性比W的强 | |
| D. | Y的气态简单氢化物的热稳定性比W的强 |
8.NM3是处于临床试验阶段的小分子抗癌药物,分子结构如图,下列说法中正确的是( )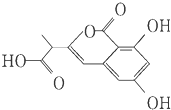
0 167668 167676 167682 167686 167692 167694 167698 167704 167706 167712 167718 167722 167724 167728 167734 167736 167742 167746 167748 167752 167754 167758 167760 167762 167763 167764 167766 167767 167768 167770 167772 167776 167778 167782 167784 167788 167794 167796 167802 167806 167808 167812 167818 167824 167826 167832 167836 167838 167844 167848 167854 167862 203614

| A. | 该有机物中含一个手性碳原子 | |
| B. | 1 mol该有机物最多可以和3 mol NaOH反应 | |
| C. | 该有机物能发生水解反应 | |
| D. | 该有机物容易发生加成、取代、消去等反应 |
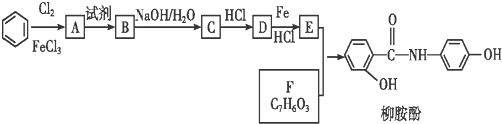
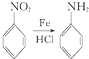
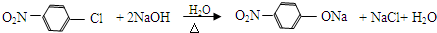
 .
.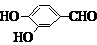 、
、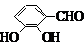 、
、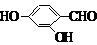 、
、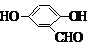 (其中三种)(写出3种).
(其中三种)(写出3种).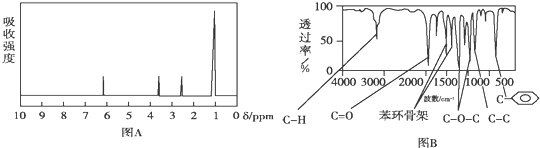
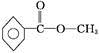 .
.