题目内容
17.下列反应中,反应后固体物质增重的是( )| A. | 高温灼烧CuO固体 | B. | 二氧化碳通过Na2O2粉末 | ||
| C. | 硫粉与铁粉混合加热 | D. | 将金属Cu投入FeCl3溶液中 |
分析 A.氧化铜高温反应生成氧化亚铜和氧气,方程式为:4CuO$\frac{\underline{\;高温\;}}{\;}$2Cu2O+O2;
B.依据二氧化碳与过氧化钠反应方程式2Na2O2+2CO2=2Na2CO3+O2,结合差量法计算解答;
C.硫粉与铁粉加热发生化合反应生成硫化亚铁;
D.铜与氯化铁溶液反应生成氯化亚铁.
解答 解:A.高温灼烧CuO固体,生成固体氧化亚铜和氧气,氧气逸出,所以固体质量减小,故A错误;
B.二氧化碳通过na2o2粉末发生的反应为:2Na2O2+2CO2=2Na2CO3+O2,固体由过氧化钠变为碳酸钠,固体质量增加,故B正确;
C.硫粉与铁粉加热发生化合反应生成硫化亚铁,S+Fe$\frac{\underline{\;\;△\;\;}}{\;}$FeS,依据质量守恒定律可知反应前后固体质量不变,故C错误;
D.铜与氯化铁溶液反应生成氯化亚铁,反应方程式:Cu+2FeCl3=CuCl2+2FeCl2,固体铜全部溶解,质量减少,故D错误;
故选:B.
点评 本题考查了有关方程式的计算,明确发生的化学反应是解题关键,题目难度不大.

练习册系列答案
相关题目
7.下列叙述错误的是( )
| A. | 活性炭、SO2、Na2O2都能使品红溶液褪色,但原理不同 | |
| B. | FeO在空气中受热会迅速转变为Fe2O3 | |
| C. | Na2SiO3溶液俗称水玻璃,可用于制备硅胶和木材防火剂 | |
| D. | 制作“毒豆芽”所用的亚硝酸钠、“小苏打水”中的碳酸氢钠都属于钠盐 |
5.过量的下列溶液与水杨酸( )反应能得到化学式为C7H5O3Na的是( )
)反应能得到化学式为C7H5O3Na的是( )
 )反应能得到化学式为C7H5O3Na的是( )
)反应能得到化学式为C7H5O3Na的是( )| A. | NaHCO3溶液 | B. | Na2CO3溶液 | C. | NaOH溶液 | D. | NaCl溶液 |
12.能在水溶液中大量共存的离子组是( )
| A. | H+、Fe3+、ClO-、Cl- | B. | H+、NH4+、Fe2+、NO3- | ||
| C. | Ag+、K+、Cl-、SO42- | D. | K+、AlO2-、Cl-、OH- |
19.下列关于电解质溶液的叙述正确的是( )
| A. | pH均为4的H2SO4、NH4Cl溶液中,水的电离程度相同 | |
| B. | 等pH的NaOH溶液与NH3•H2O 稀释后pH的变化如右图所示,则曲线I表示的是NaOH溶液的稀释 | |
| C. | 1mol/LNa2CO3溶液中存在:c(Na+)=2c(CO32- )+2c(HCO3-) | |
| D. | 向某温度的氨水中通入盐酸,则氨水的电离常数增大 |
20.用NA表示阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 23g由NO2和N2O4组成的混合气体中含有的氮原子数为0.5NA | |
| B. | 1.12L乙烯能与含0.05NA个溴分子的CCl4溶液恰好完全反应 | |
| C. | 1L0.1mol•L-1Fe2(SO4)3溶液中,Fe3+的数目为0.2NA | |
| D. | 7.8gNa2O2与水完全反应时转移的电子数为0.2NA |
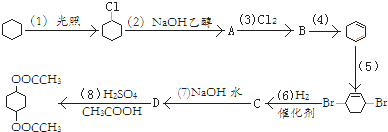
 ,取代反应
,取代反应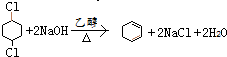 ,消去反应
,消去反应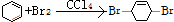 ,加成反应
,加成反应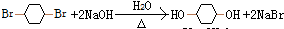 ,取代反应(水解反应)
,取代反应(水解反应)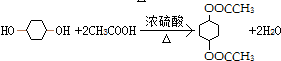 ,取代反应(酯化反应).
,取代反应(酯化反应).