16.常温下,以下溶液中c(H+)最小的是( )
| A. | pH=0的某溶液 | B. | 0.1 mol•L-1 NaOH 溶液 | ||
| C. | 0.1mol•L-1 HCl 溶液 | D. | 0.1 mol•L-1的 NaCl 溶液 |
15.下列说法正确的是:( )
①电解质在水中电离时都存在电离平衡;
②升高温度,KW增大,纯水pH不变;
③加水稀释醋酸溶液能促进醋酸电离;
④25℃向水中加入少量稀硫酸,c(H+)增大,KW不变;
⑤氯水和食盐水都能导电,所以Cl2和NaCl都是电解质;
⑥升高温度能促进弱电解质的电离;
⑦强电解质溶液的导电能力比弱电解质溶液的导电能力强.
①电解质在水中电离时都存在电离平衡;
②升高温度,KW增大,纯水pH不变;
③加水稀释醋酸溶液能促进醋酸电离;
④25℃向水中加入少量稀硫酸,c(H+)增大,KW不变;
⑤氯水和食盐水都能导电,所以Cl2和NaCl都是电解质;
⑥升高温度能促进弱电解质的电离;
⑦强电解质溶液的导电能力比弱电解质溶液的导电能力强.
| A. | ①②⑤⑦ | B. | ②③④⑤⑥ | C. | ③④⑥ | D. | ②③④⑥⑦ |
14.如图中表示外界条件(T、P)的变化对下列反应的影响L(s)+G(g)?2R(g);△H>0,y轴表示的是( )
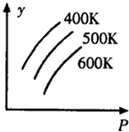

| A. | 平衡时,混合气体中R的百分含量 | B. | 平衡时,混合气中G的百分含量 | ||
| C. | G的转化率 | D. | L的转化率 |
13.下列叙述是某同学利用教材中的一些数据作出的判断,其中正确的是( )
| A. | 利用焓变或熵变的数据一定都能单独判断反应的自发性 | |
| B. | 利用沸点数据推测一些液体混合物分离开来的可能性 | |
| C. | 利用反应热数据的大小判断不同反应的反应速率的大小 | |
| D. | 利用溶液的pH与7的大小关系来判断任何温度下溶液的酸碱性 |
12.100mL 6mol•L-1H2SO4跟过量锌粉反应,在一定温度下,为了减缓反应速率,但又不影响生成氢气的总量,可向反应物中加入适量下列物质中的:①硫酸钠固体 ②水③硫酸钾溶液④硝酸钾溶液⑤醋酸钠固体⑥硫酸铜固体( )
| A. | ②③⑤ | B. | ①④⑤ | C. | ②③⑥ | D. | ③④⑥ |
11.下列各组物质中,都是强电解质的是( )
| A. | HBr、Cu(OH)2、BaSO4 | B. | NaOH、Ca(OH)2、NH3•H2O | ||
| C. | HClO、NaF、Ba(OH)2 | D. | NH4Cl、CH3COONa、Na2S |
8.表是元素周期表的短周期部分,表中字母分别表示一种元素.请回答下列问题:
(1)F元素在周期表中的位置是第三周期第ⅢA族.
(2)写出BA4的电子式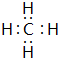 .
.
(3)用电子式表示离子化合物E2D的形成过程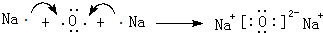 .
.
(4)C和D两种元素氢化物的稳定性更强的是H2O(填物质的化学式).
| A | |||||||
| B | C | D | |||||
| E | F | G | |||||
(2)写出BA4的电子式
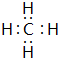 .
.(3)用电子式表示离子化合物E2D的形成过程
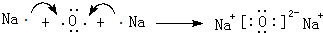 .
.(4)C和D两种元素氢化物的稳定性更强的是H2O(填物质的化学式).
7.下列有关元素性质递变情况的叙述中,正确的是( )
0 167602 167610 167616 167620 167626 167628 167632 167638 167640 167646 167652 167656 167658 167662 167668 167670 167676 167680 167682 167686 167688 167692 167694 167696 167697 167698 167700 167701 167702 167704 167706 167710 167712 167716 167718 167722 167728 167730 167736 167740 167742 167746 167752 167758 167760 167766 167770 167772 167778 167782 167788 167796 203614
| A. | Li、Be、B原子最外层电子数依次减少 | |
| B. | P、S、Cl元素最高正价依次降低 | |
| C. | Na、K、Rb的金属性依次增强 | |
| D. | N、O、F原子半径依次增大 |
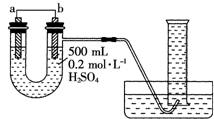 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题: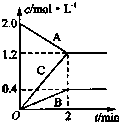 如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答:
如图表示的是在800℃时,含有A、B、C三种气体的体系中各物质浓度随时间变化的情况,请回答: