19.${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、${\;}_{1}^{3}$H、H+、H2是( )
| A. | 氢的五种不同粒子 | B. | 五种氢元素 | ||
| C. | 氢的五种同素异形体 | D. | 氢元素的五种同位素 |
18.若pH=3的酸溶液和pH=11的碱溶液等体积混合后溶液呈碱性,其原因可能是( )
| A. | 生成了一种弱酸强碱盐 | B. | 弱酸溶液和强碱溶液反应 | ||
| C. | 强酸溶液和弱碱溶液反应 | D. | 一元强酸溶液和二元强碱溶液反应 |
17.镁条和铝片为电极,并用导线连接同时插入NaOH溶液中,下列说法正确的是( )
| A. | 镁条作负极,电极反应:Mg-2e-=Mg2+ | |
| B. | 铝片作负极,电极反应:Al+4OH--3e--=[Al(OH)4]- | |
| C. | 电流从Al电极沿导线流向Mg电极 | |
| D. | 铝片上有气泡产生 |
16.四种短周期元素的性质或结构信息如下表,下列结论中错误的是( )
| 元素 | W | X | Y | Z |
| 性质或结构信息 | 单质制成的高压灯,发出的黄光透雾力强、射程远. | 工业上通过分离液态空气获得其单质.原子的最外层未达到稳定结构. | 单质常温常压下是气体,原子的M层差一个电子达稳定结构. | +2价阳离子的核外电子排布与氖原子相同. |
| A. | 上表中与W属于同一周期的元素是Z和Y | |
| B. | Z和Y形成的化合物属于离子化合物 | |
| C. | X的氢化物常温、常压下一定为液体 | |
| D. | Y单质为有色气体,具有强氧化性 |
15.下列说法正确的是( )
| A. | 含有共价键的化合物不一定是共价化合物 | |
| B. | 全部由非金属元素组成的化合物一定是共价化合物 | |
| C. | 由共价键形成的分子一定是共价化合物 | |
| D. | 硫酸分子中有H+和SO42-两种离子 |
14.意大利一所大学的科学家制造出了由4个氧原子构成的一种新型分子.下列说法正确的是( )
| A. | 该分子是氧元素的一种同位素 | B. | 该分子的摩尔质量为64 g | ||
| C. | 该物质与氧气互为同素异形体 | D. | 该物质是一种氧化物 |
13.同一周期中,X、Y、Z三种元素,其气态氢化物稳定性按X、Y、Z的顺序不断增强,下列说法正确的是( )
| A. | 非金属性X>Y>Z | |
| B. | 原子半径X>Y>Z | |
| C. | 它们最高价氧化物水化物的酸性按X、Y、Z顺序增强 | |
| D. | 气态氢化物的还原性按X、Y、Z顺序增强 |
12.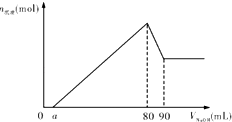 将一块镁铝的合金投入1mo1•L-1的一定体积的稀盐酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位mL)的关系如图.下列说法中不正确的是( )
将一块镁铝的合金投入1mo1•L-1的一定体积的稀盐酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位mL)的关系如图.下列说法中不正确的是( )
 将一块镁铝的合金投入1mo1•L-1的一定体积的稀盐酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位mL)的关系如图.下列说法中不正确的是( )
将一块镁铝的合金投入1mo1•L-1的一定体积的稀盐酸中,待合金完全溶解后,往溶液里滴入1mo1•L-1的NaOH溶液,生成沉淀物质的量与加入NaOH溶液体积(单位mL)的关系如图.下列说法中不正确的是( )| A. | 由图可以确定该镁铝合金中铝的质量为0.27g | |
| B. | 当滴入1mo1•L-1的NaOH溶液85mL时,所得沉淀为Mg(OH)2和Al(OH)3 | |
| C. | 由图可以确定a的取值范围为:0≤a≤50 | |
| D. | 由图可以确定该合金中镁铝物质的量之比0<$\frac{n(Mg)}{n(AI)}$<2.5 |
10.在铜-锌-硫酸构成的原电池中,当导线中有1mol电子通过时,理论上的两极变化是( )
①锌片溶解32.5g ②锌片增重32.5g ③铜片上析出1gH2 ④铜片上析出1mol H2.
0 167559 167567 167573 167577 167583 167585 167589 167595 167597 167603 167609 167613 167615 167619 167625 167627 167633 167637 167639 167643 167645 167649 167651 167653 167654 167655 167657 167658 167659 167661 167663 167667 167669 167673 167675 167679 167685 167687 167693 167697 167699 167703 167709 167715 167717 167723 167727 167729 167735 167739 167745 167753 203614
①锌片溶解32.5g ②锌片增重32.5g ③铜片上析出1gH2 ④铜片上析出1mol H2.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
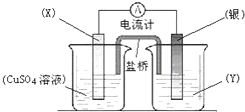 依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.
依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池如图所示.