题目内容
15.下列说法正确的是( )| A. | 含有共价键的化合物不一定是共价化合物 | |
| B. | 全部由非金属元素组成的化合物一定是共价化合物 | |
| C. | 由共价键形成的分子一定是共价化合物 | |
| D. | 硫酸分子中有H+和SO42-两种离子 |
分析 A、离子化合物中可能含有共价键;
B、非金属元素也可能形成离子化合物;
C、单质分子中也可能含有共价键;
D、硫酸分子中没有离子.
解答 解:A、含有共价键的化合物不一定是共价化合物,离子化合物中可能含有共价键,如过氧化钠、氯化铵,故A正确;
B、非金属元素也可能形成离子化合物,如氯化铵是由非金属元素组成的离子化合物,故B错误;
C、单质分子中也可能含有共价键,如氢气中含有共价键,但是氢气属于单质不是化合物,故C错误;
D、硫酸分子中没有离子,硫酸属于分子晶体,是由分子构成的化合物,没有离子,故D错误;
故选A.
点评 本题考查了共价化合物的概念,学生在解决这类型的题目的同时要充分掌握概念,题目难度不大.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
5.下列有机物的命名正确的是( )
| A. | 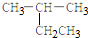 2-乙基乙烷 | B. | 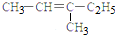 3-甲基-3-戊稀 3-甲基-3-戊稀 | C. | 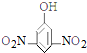 2,4-二硝基苯酚 2,4-二硝基苯酚 | D. |  2,3-丁二醇 |
3.如图是酸性氢氧燃料电池构造示意图.关于该电池的说法不正确的是( )
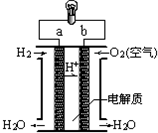

| A. | a极是负极 | |
| B. | 电流由b通过灯泡流向a | |
| C. | 正极的电极反应是:O2+2H2O+4e-═4OH- | |
| D. | 氢氧燃料电池是环保电池 |
10.在铜-锌-硫酸构成的原电池中,当导线中有1mol电子通过时,理论上的两极变化是( )
①锌片溶解32.5g ②锌片增重32.5g ③铜片上析出1gH2 ④铜片上析出1mol H2.
①锌片溶解32.5g ②锌片增重32.5g ③铜片上析出1gH2 ④铜片上析出1mol H2.
| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
20.钾的金属活动性比钠强,根本原因是( )
| A. | 钾的密度比钠的小 | B. | 加热时,钾比钠更易气化 | ||
| C. | 钾与水反应比钠与水反应更剧烈 | D. | 钾原子的电子层比钠原子多一层 |
7.1.0L 1.00mol•L-1H2SO4溶液与2.00L 1.00mol•L-1NaOH溶液完全反应,放出114.6kJ热量,则可推算出该条件下酸与碱反应的中和热为( )
| A. | 57.3 kJ•mol-1 | B. | 114.9 kJ•mol-1 | C. | 171.9 kJ•mol-1 | D. | 229.2 kJ•mol-1 |
4.下列关于电化学的说法中错误的是( )
| A. | 原电池的负极、电解池的阳极均发生氧化反应 | |
| B. | 原电池将化学能转化为电能,电解池将电能转化为化学能 | |
| C. | 电解水制取H2和O2时,为了增强导电性,可加入NaOH、NaCl、H2SO4 | |
| D. | 利用原电池原理可制备化学电源,利用电解池原理可制备化学物质 |
