4.25℃、101kPa下,反应2N2O5(g)=4NO2(g)+O2(g)△H=+56.7kJ/mol能自发进行的原因是( )
| A. | 是吸热反应 | B. | 是放热反应 | ||
| C. | 是熵减小的反应 | D. | 熵增效应大于热效应 |
3.下列说法正确的是( )
| A. | 易溶于水的电解质一定是强电解质,难溶于水的电解质一定是弱电解质 | |
| B. | 强电解质溶液的导电能力一定比弱电解质溶液强 | |
| C. | NaCl溶液在电流的作用下电离成钠离子和氯离子 | |
| D. | 氯化钠晶体不导电是由于氯化钠晶体中不存在自由移动的离子 |
2.能够充分说明在恒温下的密闭容器中,反应 2SO2+O2?2SO3 已经达到平衡状态的标志是( )
| A. | 容器中SO2、O2和SO3共存 | |
| B. | SO2和SO3的物质的量浓度相等 | |
| C. | 容器中SO2、O2、SO3的物质的量之比为2:1:2 | |
| D. | 反应器内压强不再随时间发生变化 |
16.巴豆酸是一种对胃肠道有强烈刺激性、对呼吸中枢和心脏有麻痹作用的有机酸,其结构简式为CH3-CH=CH-COOH,现有①氯化氢 ②溴水 ③纯碱溶液 ④乙醇 ⑤酸性高锰酸钾溶液试根据其结构特点判断在一定条件下能与巴豆酸反应的物质是( )
| A. | 只有②④⑤ | B. | 只有①③④ | C. | 只有①②③④ | D. | 全部 |
15.已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)$?_{催化剂}^{高温、高压}$2NH3(g)△H=-92.4kJ•mol-1,则N≡N键的键能是( )
0 167519 167527 167533 167537 167543 167545 167549 167555 167557 167563 167569 167573 167575 167579 167585 167587 167593 167597 167599 167603 167605 167609 167611 167613 167614 167615 167617 167618 167619 167621 167623 167627 167629 167633 167635 167639 167645 167647 167653 167657 167659 167663 167669 167675 167677 167683 167687 167689 167695 167699 167705 167713 203614
| A. | 431 kJ•mol-1 | B. | 946 kJ•mol-1 | C. | 649 kJ•mol-1 | D. | 896 kJ•mol-1 |
 ;
;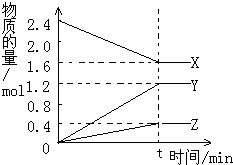 在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示:
在2L容器中3种物质间进行反应,X、Y、Z的物质的量随时间的变化曲线如图.反应在t时到达平衡,依图所示: