4.密闭的真空容器中放入一定量CaO2固体,发生反应2CaO2(s)?2CaO(s)+O2(g)并达到平衡.保持温度不变,缩小容器容积为原来的三分之二,重新平衡后,下列叙述正确的是( )
| A. | 平衡常数减小 | B. | CaO的量减少 | C. | 氧气浓度不变 | D. | CaO2的量不变 |
3.亚氯酸钠(NaClO2)是一种性能优良的漂白剂,但在酸性溶液发生分解:5HClO2→4ClO2+H++Cl-+2H2O.
向亚氯酸钠溶液中加入盐酸,反应剧烈.若将盐酸改为pH相同的稀硫酸,开始时反应缓慢,稍后产生气体速度较快,速度变化的原因是( )
向亚氯酸钠溶液中加入盐酸,反应剧烈.若将盐酸改为pH相同的稀硫酸,开始时反应缓慢,稍后产生气体速度较快,速度变化的原因是( )
| A. | 逸出ClO2使生成物浓度降低 | B. | 酸使HClO2的分解加速 | ||
| C. | 溶液中的H+起催化作用 | D. | 溶液中的Cl-起催化作用 |
2.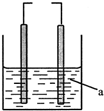 如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
①2H++2e→H2↑ ②O2+4e+2H2O→4OH- ③2Cl--2e→Cl2↑
 如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )
如图的装置,左为铁电极,右为石墨电极,a为水或某种溶液.若两电极直接连接或外接电源,石墨上可能发生的反应是( )①2H++2e→H2↑ ②O2+4e+2H2O→4OH- ③2Cl--2e→Cl2↑
| A. | ① | B. | ② | C. | ①② | D. | ①②③ |
1.如表实验所用的试剂不合理的是( )
| 选项 | 实验目的 | 所用试剂 |
| A | 比较Fe3+和Cu2+的氧化性 | FeCl3溶液和Cu |
| B | 比较镁和铝的金属性 | MgCl2溶液、AlCl3溶液、NaOH溶液 |
| C | 比较硫和氯的非金属性 | 氢硫酸、氯气 |
| D | 比较苯酚和碳酸的酸性 | 0.1mol/L苯酚钠、0.1mol/L碳酸钠溶液pH试纸 |
| A. | A | B. | B | C. | C | D. | D |
20.根据如表数据,则与HClO3比,HClO具有的是( )
| Cl-O键键长(pm) | Cl-O键能(KJ/mol) | |
| HClO | 170 | 209 |
| HClO3 | 157 | 244 |
| A. | 更高的沸点 | B. | 更强的酸性 | ||
| C. | Cl-O断裂放出的能量更少 | D. | 更易放出原子氧 |
19.碳元素的一种单质的化学式为C68,则关于C68的叙述错误的是( )
| A. | 属分子晶体 | B. | 可溶于CCl4 | C. | 固态可导电 | D. | 熔点高于C60 |
18.在对电子运动状态的描述中,确定一个“轨道”的方面包括( )
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子的自旋状态.
0 167466 167474 167480 167484 167490 167492 167496 167502 167504 167510 167516 167520 167522 167526 167532 167534 167540 167544 167546 167550 167552 167556 167558 167560 167561 167562 167564 167565 167566 167568 167570 167574 167576 167580 167582 167586 167592 167594 167600 167604 167606 167610 167616 167622 167624 167630 167634 167636 167642 167646 167652 167660 203614
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子的自旋状态.
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ① |