6. 分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )
 分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )
分析化学中常用X射线研究晶体结构,有一种蓝色晶体可表示为:MxFey(CN)z,研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN一位于立方体的棱上,其晶体中的阴离子结构如图示,下列说法正确的是( )| A. | 该晶体是原子晶体 | |
| B. | M的离子位于上述立方体的面心,呈+2价 | |
| C. | M的离子位于上述立方体的体心,呈+1价,且M+空缺率(体心中没有M+的占总体心的百分比)为50% | |
| D. | 晶体的化学式可表示为MFe2(CN)3,且M为+1价 |
5.Co(Ⅲ)的八面体配合物CoClm•nNH3,若1mol 配合物与足量AgNO3溶液作用生成1mol AgCl沉淀,则m、n的值是( )
| A. | m=1,n=5 | B. | m=3,n=4 | C. | m=5,n=1 | D. | m=3,n=3 |
4.下列对分子的性质的解释中,不正确的是( )
| A. | 水很稳定(1000℃以上才会部分分解)是因为水中含有大量的氢键所致 | |
| B. | 乳酸(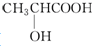 )有一对手性异构体,因为其分子中含有一个手性碳原子 )有一对手性异构体,因为其分子中含有一个手性碳原子 | |
| C. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| D. | 酸性:H3PO4>HClO,因为H3PO4的非羟基氧原子数比HClO的多 |
3.“莫斯科2009年7月28日电,27日夜间,位于莫斯科郊外的杜伯纳国际联合核研究所的专家们启动新元素合成实验,如果顺利的话,实验结束时将会合成门捷列夫元素周期表上的第117号新元素”.下列有关该元素的说法正确的是( )
| A. | 117 g该元素原子的物质的量为1 mol | |
| B. | 该元素一定为非金属元素 | |
| C. | 该元素在地球上的含量十分丰富 | |
| D. | 该元素的金属性可能比非金属性更明显 |
1.下列关于乙酸的叙述中不正确的是( )
| A. | 普通的食醋中含3%~5%(质量分数)的乙酸 | |
| B. | 醋酸是一种弱酸,其酸性比碳酸更弱 | |
| C. | 可以用醋除去烧开水的壶内壁的水垢 | |
| D. | 在一定条件下,乙酸能与乙醇发生酯化反应 |
20.部分弱酸的电离平衡常数如表,下列表述肯定正确的是( )
| 弱酸 | H2CO3 | H2SO3 | HClO |
| 电离平衡常数 (25℃) | K1=4.30×10-7 | K1=1.54×10-2 | K=2.95×10-8 |
| K2=5.61×10-11 | K2=1.02×10-7 |
| A. | 相同温度时三种溶液的pH关系:Na2CO3>NaClO>Na2SO3 | |
| B. | ClO-+H2O+CO2→HClO+HCO3- | |
| C. | 2ClO-+SO2+H2O→2HClO+SO32- | |
| D. | 等体积、等物质的量浓度的HClO和Na2CO3混合后溶液呈中性 |
19.下列说法正确的是( )
0 167334 167342 167348 167352 167358 167360 167364 167370 167372 167378 167384 167388 167390 167394 167400 167402 167408 167412 167414 167418 167420 167424 167426 167428 167429 167430 167432 167433 167434 167436 167438 167442 167444 167448 167450 167454 167460 167462 167468 167472 167474 167478 167484 167490 167492 167498 167502 167504 167510 167514 167520 167528 203614
| A. | 230Th和232Th是钍的两种同素异形体 | |
| B. | H2与T2互为同位素 | |
| C. | 甲醇与乙醇互为同系物 | |
| D. | 乙酸乙酯与丁酸互为同分异构体 |
 化合物Na2O的晶胞如图.
化合物Na2O的晶胞如图. 是一种环保型的新涂料,其合成路线如下图所示:
是一种环保型的新涂料,其合成路线如下图所示:
 .
.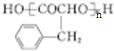 .
. .
.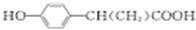 (写出其中一种的结构简式).
(写出其中一种的结构简式).
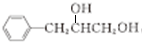 ,试剂G的化学式H2.
,试剂G的化学式H2.
 .
. .
. .
.