题目内容
【题目】请回答下列问题:
(1)基态Si原子中,电子占据的最高能层符号为___,该能层具有的原子轨道数为___。
(2)BF3与一定量的水形成(H2O)2BF3晶体Q,Q在一定条件下可转化为R:

晶体Q中各种微粒间的作用力有____(填序号)。
a 离子键 b 共价键 c 配位键 d 氢键
(3)第一电离能I1(Zn)___I1(Cu)(填“大于”或“小于”),原因是______。
(4)石墨烯(如图a)是一种由单层碳原子构成的平面结构新型碳材料,石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图b)。
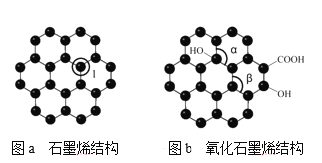
图a中,1号C与相邻C形成σ键的个数为____,图b中键角α___键角β。(填“>”、“<”或“=” );
【答案】M 9 bcd 大于 Zn核外电子排布为全满稳定结构,较难失电子 3 <
【解析】
(2)非金属元素原子之间易形成共价键,含有空轨道的原子和含有孤电子对的原子之间易形成配位键,水分子中的O原子和其它分子中的H原子易形成氢键;
(3)同周期相邻元素比较第一电离能大小时要注意核外电子排布;
(4)单键均为σ键,双键中有一个σ键;根据C原子的杂化方式判断键角大小。
(1)基态Si原子核外有三个电子层,离核远的能量高,故占据的最高能层为第三能层,符号为M;第三能层有s、p、d三种轨道,轨道数分别为1、3、5,共计9个原子轨道;
(2)晶体Q中非金属元素原子之间易形成共价键,含有B-F、O-H等共价键;B原子含有空轨道、O原子含有孤电子对,所以B原子和O原子之间存在配位键;水分子中的O原子和其它分子中的H原子易形成氢键,所以选bcd;
(3)Zn核外电子排布为全满稳定结构,较难失电子,所以Zn的第一电离能大于Cu;
(4)每个C原子要形成4个共价键,根据图a知,每个C原子形成2个共价单键、1个共价双键,共价单键为σ键、共价双键中1个是σ键、1个是π键,所以图a中1号碳原子与相邻C形成3个σ键;
图b中,键角α中中心C形成3个C-C键及1个C-O键,C原子为sp3杂化,为四面体构型,而键角β中中心C原子杂化方式为sp2,为平面结构,所以键角α<键角β。

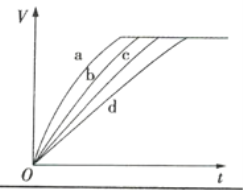
【题目】等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定反应过程中产生氢气体积V,根据相关数据所绘制的图象如图所示,则曲线a、b、c、d所对应的实验组别可能依次是( )
实验组别 | c(HCl)/(mol·L-1) | 温度/℃ | 形状(Fe) |
1 | 2.0 | 30 | 块状 |
2 | 2.5 | 30 | 块状 |
3 | 2.5 | 50 | 粉末状 |
4 | 2.5 | 30 | 粉末状 |
A.4、3、2、1B.1、2、3、4
C.3、4、2、1D.1、2、4、3
【题目】Ⅰ.氮的固定是几百年来科学家一直研究的课题。
(1)下表列举了不同温度下大气固氮和工业固氮的部分K值。
反应 | 大气固氮 N2(g)+O2(g) | 工业固氮 N2(g)+3H2(g) | |||
温度/℃ | 27 | 2000 | 25 | 400 | 450 |
K | 3.8×10﹣31 | 0.1 | 5×108 | 0.507 | 0.152 |
①分析数据可知:大气固氮反应属于_____(填“吸热”或“放热”)反应。
②分析数据可知;人类不适合大规模模拟大气固氮的原因__________________________。
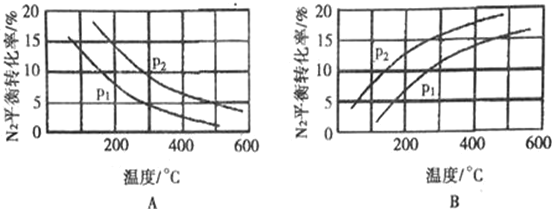
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(P1、P2)下随温度变化的曲线,如图所示的图示中,正确的是___(填“A”或“B”);比较P1、P2的大小关系:P1______P2(填“>”、“=” 或“<”)。
Ⅱ. 目前工业合成氨的原理是:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(3)在一定温度下,将1mol N2和3mol H2混合置于体积不变的密闭容器中发生反应,达到平衡状态时,测得气体总物质的量为2.8mol。达平衡时,H2的转化率α1=____。