题目内容
【题目】某溶液中可能含有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等离子
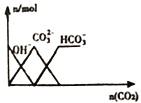
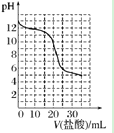
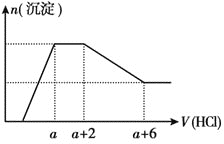
等离子![]() 当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是
当向该溶液中逐滴加入一定物质的量浓度的盐酸时,发现生成沉淀的物质的量随盐酸溶液的体积变化的图像如图所示,下列说法正确的是![]()
![]()
A.原溶液中一定含有![]()
B.反应后最终溶液中的溶质只有![]()
C.原溶液中含有![]() 与
与![]() 的物质的量之比为
的物质的量之比为![]()
D.原溶液中一定含有的阴离子是![]() 、
、![]() 、
、![]() 、
、![]()
【答案】D
【解析】
由图象可知,开始加入HCl时无沉淀生成,说明加入的HCl与溶液中![]() 的反应,则溶液中一定不会存在与氢氧根离子发生反应的离子:
的反应,则溶液中一定不会存在与氢氧根离子发生反应的离子:![]() 、
、![]() 、
、![]() ;之后开始生成沉淀且反应生成沉淀逐渐增大,说明溶液中存在
;之后开始生成沉淀且反应生成沉淀逐渐增大,说明溶液中存在![]() 、
、![]() ,继续加入盐酸沉淀量不变,消耗盐酸的离子只能是
,继续加入盐酸沉淀量不变,消耗盐酸的离子只能是![]() ,
,![]() 反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐酸,最后剩余沉淀为硅酸;硫酸根离子不能确定存在,但根据溶液的电中性可知,溶液中
反应完后继续加入盐酸,沉淀逐渐减小,到不再改变,进一步证明沉淀是氢氧化铝和硅酸沉淀,氢氧化铝沉淀溶于盐酸,最后剩余沉淀为硅酸;硫酸根离子不能确定存在,但根据溶液的电中性可知,溶液中![]() 一定存在,据以上分析一定存在
一定存在,据以上分析一定存在![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() ,一定不存在
,一定不存在![]() 、
、![]() 、
、![]() ,不确定是否存在
,不确定是否存在![]() 。
。
A.据以上分析知溶液中不确定是否存在![]() ,则原溶液中不一定含有
,则原溶液中不一定含有![]() ,故A错误;
,故A错误;
B.据以上分析知溶液中含有![]() ,则反应后形成的溶液溶质有NaCl,故B错误;
,则反应后形成的溶液溶质有NaCl,故B错误;
C.依据图象可知和碳酸根离子反应的盐酸为2体积,反应总方程式为:![]() ;氢氧化铝溶解消耗的盐酸体积为4体积,反应的离子方程式为:
;氢氧化铝溶解消耗的盐酸体积为4体积,反应的离子方程式为:![]() ;所以原溶液中含有
;所以原溶液中含有![]() 与
与![]() 的物质的量之比为
的物质的量之比为![]() ,据铝元素守恒知原溶液中含有
,据铝元素守恒知原溶液中含有![]() 与
与![]() 的物质的量比为
的物质的量比为![]() ,故C错误;
,故C错误;
D.根据以上分析可知,原溶液中一定含有的阴离子是:![]() 、
、![]() 、
、![]() 、
、![]() ,故D正确;
,故D正确;
答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、SO2等气体,严重污染空气。通过对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。
(1)已知:H2的燃烧热为285.8 kJ·mol-1 H2O(g)=H2O(l) ΔH=-44 kJ/mol
N2(g)+2O2(g)=2NO2(g) ΔH=+133 kJ/mol
①在催化剂存在下,H2还原NO2生成水蒸气和另一种无毒物质的热化学方程式为:___________________________________。
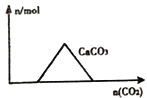
②反应2NO2(g )=N2(g)+2O2(g),设起始时容器中只有NO2,平衡时三种物质的物质的量与温度关系如图所示。

则A点时,NO2的转化率为_______________。
B点时,设容器的总压为a Pa,则平衡常数Kp为____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)向2 L密闭容器中加入2 mol CO2和6 mol H2,在适当的催化剂作用下,下列反应能自发进行:CO2(g)+3H2(g)![]() CH3OH(g) +H2O(g)。
CH3OH(g) +H2O(g)。
①该反应ΔH_______0(填“>”、“<”或“=”)
②下列叙述能说明此反应达到平衡状态的是____________。(填字母)
a.混合气体的平均相对分子质量保持不变
b.1 mol CO2生成的同时有3 mol H—H键断裂
c.CO2的转化率和H2的转化率相等
d.混合气体的密度保持不变
③反应CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g),在起始温度(T1℃)、体积相同(2L)的两密闭容器中,改变条件,反应过程中部分数据见下表:
CH3OH(g)+H2O(g),在起始温度(T1℃)、体积相同(2L)的两密闭容器中,改变条件,反应过程中部分数据见下表:
反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol | |
反应Ⅰ:恒温恒容 | 0 min | 2 | 6 | 0 | 0 |
10 min | 4.5 | ||||
20 min | 1 | ||||
30 min | 1 | ||||
反应Ⅱ:绝热恒容 | 0 min | 0 | 0 | 2 | 2 |
反应Ⅰ,前10min内的平均反应速率v(CH3OH)=____________。达到平衡时,反应Ⅰ、Ⅱ对比:平衡常数K(I)____________K(II)(填“>”、“<”或“=”);平衡时CH3OH的浓度c(I)____________c(II)(填“>”、“<”或“=”)。