题目内容
【题目】室温时,将浓度和体积分别为![]() 、
、![]() 的NaOH溶液和
的NaOH溶液和![]() 、
、![]() 的
的![]() 溶液相混合,关于该混合溶液的叙述正确的是
溶液相混合,关于该混合溶液的叙述正确的是
A.若![]() ,则一定是
,则一定是![]()
B.在任何情况下都存在![]()
C.在任何情况下都不可能存在:![]() 、
、![]()
D.若![]() ,
,![]() ,则
,则![]() 和
和![]() 浓度之和等于
浓度之和等于![]() 浓度
浓度
【答案】B
【解析】
A.当溶液呈碱性时,溶液中氢离子浓度小于氢氧根离子浓度,但混合时醋酸的物质的量不一定等于氢氧化钠的物质的量;
B.溶液呈电中性,溶液中阴阳离子所带电荷相等;
C.![]() 水解使溶液呈碱性,若
水解使溶液呈碱性,若![]() 稍过量,可使溶液为中性;
稍过量,可使溶液为中性;
D.根据物料守恒分析。
![]() 醋酸是弱酸,氢氧化钠是强碱,所以等物质的量的酸和碱混合时,溶液呈碱性,当氢氧化钠过量时溶液更呈碱性,所以当
醋酸是弱酸,氢氧化钠是强碱,所以等物质的量的酸和碱混合时,溶液呈碱性,当氢氧化钠过量时溶液更呈碱性,所以当![]() 时,则一定是
时,则一定是![]() ,故A错误;
,故A错误;
B.溶液呈电中性,溶液中阴阳离子所带电荷相等,所以得![]() ,故B正确;
,故B正确;
C.![]() 水解使溶液呈碱性,若
水解使溶液呈碱性,若![]() 稍过量,可使溶液为中性,可以存在:
稍过量,可使溶液为中性,可以存在:![]() 、
、![]() ,故C错误;
,故C错误;
D.若![]() ,
,![]() ,则从物料守恒角度,
,则从物料守恒角度,![]() ,故D错误,
,故D错误,
故选:B。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】今有室温下四种溶液,有关叙述不正确的是
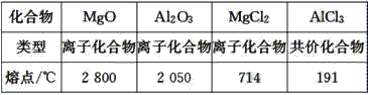
序号 | ① | ② | ③ | ④ |
pH | 11 | 11 | 3 | 3 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A. ③④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B. ②③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C. 分别加水稀释10倍,四种溶液的pH①>②>④>③
D. V1L④与V2L①溶液混合后,若混合后溶液pH=7,则V1<V2