题目内容
5.下列应用或事实与胶体的性质没有关系的是( )| A. | 在河流入海口处易形成三角州 | |
| B. | 用石膏或盐卤点制豆腐 | |
| C. | 尿毒症患者做“血液透析” | |
| D. | 在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色沉淀 |
分析 A.江河中的泥沙属于胶体分散系;
B.胶体加入电解质发生聚沉;
C.血液是胶体;
D.红褐色沉淀是生成的氢氧化铁,不是胶体.
解答 解:A.江河中的泥沙属于胶体分散系,江河入海口三角洲的形成与胶体的聚沉性质有关,故A错误;
B.用石膏或盐卤点制豆腐,利用的是胶体的聚沉,和胶体性质有关,故B错误;
C.血液是胶体,能发生渗析,与胶体有关,故C错误;
D.在FeCl3溶液中滴加NaOH溶液出现红褐色沉淀,发生的是复分解反应,与胶体无关,故D正确.
故选D.
点评 本题考查了胶体性质的应用,主要考查胶体的聚沉、胶体的分散质微粒直径,渗析等,熟练掌握胶体性质是解题关键,较简单.

练习册系列答案
相关题目
15.下列溶液一定呈酸性的是( )
| A. | c(H+)=10-6 mol•L-1的溶液 | B. | pH<7的溶液 | ||
| C. | c(H+)>c(OH-)的溶液 | D. | 滴加酚酞显无色的溶液 |
16.下列变化需要加入氧化剂才能实现的是( )
| A. | S2-→HS- | B. | Cu2+→Cu | C. | S→S2- | D. | Cl-→Cl2 |
20.下列物质所含分子数最多的是( )
| A. | 标准状况下22.4L CH4 | B. | 28g N2( N2的摩尔质量为28g/mol ) | ||
| C. | 1.5mol H2O | D. | 6.02×1023个NH3 |
10.常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是( )
| A. | b一定显中性 | B. | a可能显酸性或碱性 | ||
| C. | a不可能显酸性 | D. | b可能显碱性或酸性 |
17.CuI是一种白色难溶于水的固体,以石墨作阴极,铜为阳极组成电解池,含有酚酞和淀粉KI的溶液作电解液,电解开始一段时间,阴极区溶液变红,阳极区为无色,电解相当长时间后,阳极区才呈深蓝色,则电解开始阶段的电极反应为( )
| A. | 阳极:Cu-2e-═Cu2+ 阴极:Cu2++2e-═Cu | |
| B. | 阳极:2Cu+2I--2e-═2CuI 阴极:2H++2e-═H2↑ | |
| C. | 阳极:2I--2e-═I2 阴极:2H++2e-═H2↑ | |
| D. | 阳极:4OH--4e-═2H2O+O2↑ 阴极:4H++4e-═2H2↑ |
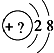 某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断.
某同学在画某种元素的一种单核微粒的结构示意图时,忘记在圆圈内标出其质子数,请你根据下面的提示做出自己的判断. ;
;