题目内容
15.为了证明某晶体中含有NH4+、K+、SO42-和H2O,下列实验叙述中不正确的是( )| A. | 取少量晶体放入试管中,加热,若试管口上蘸有少量无水硫酸铜粉末的脱脂棉变蓝,则可证明晶体中含有结晶水 | |
| B. | 取少量晶体溶于水,加入少量NaOH溶液,加热,在试管口用湿润的蓝色石蕊试纸检验,若变红,则可证明晶体的成分中含有NH4+ | |
| C. | 取少量晶体溶于水,加适量稀盐酸,无现象,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42- | |
| D. | 取少量晶体溶于水,用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,不能证明晶体中无K+ |
分析 A.加热失去结晶水,然后用无水硫酸铜检验水;
B.检验氨气,应该用湿润的红色石蕊试纸;
C.依据硫酸根离子的检验方法分析判断;
D.确定焰色反应中是否含有钾离子,需要透过蓝色钴玻璃观察火焰颜色.
解答 解:A.晶体加热后生成水,若无水硫酸铜变蓝,则证明晶体中含结晶水,故A正确;
B.向某无色溶液中加入浓NaOH溶液,加热试管,检验氨气,利用湿润的红色石蕊试纸,试纸变蓝,则说明原溶液中一定含NH4+,不是用蓝色石蕊试纸检验,故B错误;
C.加少量稀盐酸,无现象,排除了干扰离子,再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO42-,故C正确;
D.取少量晶体溶于水,用洁净的铂丝蘸取少量溶液在酒精灯火焰上灼烧,火焰呈黄色,说明含有钠离子,若证明是否含有钾离子,则需要透过蓝色钴玻璃观察,所以该现象不能证明晶体中无K+,故D正确;
故选B.
点评 本题考查常见离子的检验方法,题目难度中等,熟练掌握常见离子的性质及检验方法为解答的关键,试题有利于提高学生的分析能力及灵活应用基础知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.25℃时,水中存在电离平衡:H2O═H++OH-△H>0.下列叙述正确的是( )
| A. | 将水加热,Kw增大,pH不变 | |
| B. | 向水中加入少量NaHSO4固体,溶液的c(H+)增大,水电离的c(H+)降低 | |
| C. | 向水中加入少量NaOH固体,平衡逆向移动,溶液的c(OH-)降低 | |
| D. | 向水中加入少量NH4Cl固体,平衡正向移动,溶液的c(OH-)增大 |
3.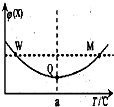 在某恒容密闭容器中充入一定量 X(g)和 Y(g),发生反应2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中 X 的体积分数与温度的 关系如图.下列推断正确的是( )
在某恒容密闭容器中充入一定量 X(g)和 Y(g),发生反应2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中 X 的体积分数与温度的 关系如图.下列推断正确的是( )
 在某恒容密闭容器中充入一定量 X(g)和 Y(g),发生反应2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中 X 的体积分数与温度的 关系如图.下列推断正确的是( )
在某恒容密闭容器中充入一定量 X(g)和 Y(g),发生反应2X(g)+Y(g)?3Z(g)△H,反应过程中持续升高温度,测得混合体系中 X 的体积分数与温度的 关系如图.下列推断正确的是( )| A. | M 点时,Y 的转化率最大 | |
| B. | 升高温度,平衡常数减小 | |
| C. | 平衡后充入 Z 达到新平衡时 Z 的体积分数增大 | |
| D. | W,M 两点 Y 的正反应速率相等 |
10.下列说法正确的是( )
| A. | 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸 | |
| B. | 酸性氧化物都是非金属氧化物 | |
| C. | Na2O熔融状态下能导电,所以Na2O是电解质 | |
| D. | 胶体区别于其他分散系的本质特征是产生丁达尔效应 |
7.对于 90℃的纯水,以下认识正确的是( )
| A. | c (H+)>10-7 mol/L>c (OH-) pH<7 显中性 | |
| B. | c (H+)=c (OH-)>10-7 mol/L pH<7 显中性 | |
| C. | c (H+)>10-7 mol/L>c (OH-) pH<7 显酸性 | |
| D. | c (H+)=c (OH-)>10-7 mol/L pH=7 显中性 |
4.工业上制取镁单质,常将镁蒸气在下列哪种气体环境中冷却( )
①O2
②CO2
③空气
④Ar
⑤N2.
①O2
②CO2
③空气
④Ar
⑤N2.
| A. | ②④⑤ | B. | 只有④ | C. | ③④⑤ | D. | 全部 |
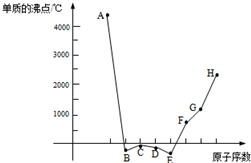 A、B、C、D、E、F、G、H八种短周期元素,其单质的沸点如图所示.
A、B、C、D、E、F、G、H八种短周期元素,其单质的沸点如图所示.