题目内容
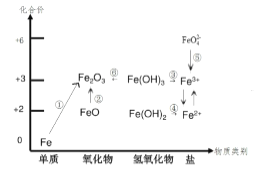
【题目】某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:
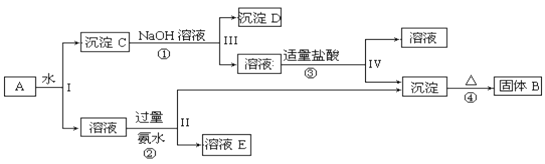
据此回答下列问题:
(1)I、II、III、IV四步操作采取的分离方法是___________________。
(2)根据上述框图反应关系,写出下列B、C、E所含物质的化学式沉淀固体B________________;C______________________;E_______________
(3)写出①、②、④三个反应方程式(有离子反应的写离子方程式,没有的写化学方程式)
①____________________________ ② ____________________________
④__________________________
【答案】过滤 Al2O3 Al2O3、Fe2O3 K2SO4、(NH4)2SO4 Al2O3+2OH- = 2AlO2- + H2O Al3+ +3NH3·H2O=Al(OH)3↓+3NH4+ 2Al(OH)3![]() Al2O3+3H2O
Al2O3+3H2O
【解析】
混合物A加水后,![]() 和
和![]() 均不溶于水,变成沉淀C,溶液中为
均不溶于水,变成沉淀C,溶液中为![]() ,KAl(SO4)2溶液中加入过量氨水后铝离子会转变成
,KAl(SO4)2溶液中加入过量氨水后铝离子会转变成![]() ,溶液中含
,溶液中含![]() 和
和![]() 、过量氨水,即溶液E。向沉淀C即
、过量氨水,即溶液E。向沉淀C即![]() 和
和![]() 中加入NaOH溶液,只有
中加入NaOH溶液,只有![]() 会溶于NaOH变成
会溶于NaOH变成![]() ,沉淀D为不溶的
,沉淀D为不溶的![]() ;向
;向![]() 溶液中加入适量盐酸可以得到
溶液中加入适量盐酸可以得到![]() 沉淀和
沉淀和![]() 溶液,最后加热
溶液,最后加热![]() 分解得到
分解得到![]() ,即固体B,据此分析作答。
,即固体B,据此分析作答。
(1)步骤I、II、III、IV均为分离不溶性沉淀和溶液,因此选用的方法为过滤;
(2)根据前面的分析,B为![]() ,C为
,C为![]() 和
和![]() 二者混合物,E为
二者混合物,E为![]() 和
和![]() 混合物;
混合物;
(3)根据题图和前面的分析来写即可:①为![]() ;②为
;②为![]() ,注意氨水不能拆;④为
,注意氨水不能拆;④为![]() ,该过程无离子反应方程式。
,该过程无离子反应方程式。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案【题目】现有部分元素的性质与原子(或分子)结构如下表:
元素编号 | 元素性质与原子(或分子)结构 |
T | 最外层电子数是次外层电子数的3倍 |
X | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Y | M层比K层少1个电子 |
Z | 第三周期元素的简单离子中半径最小 |
(1)写出这四种元素的元素符号:T_______;X_______;Y_______;Z_______。
(2)写出元素T的原子结构示意图_____________________________
(3)元素Y与元素Z相比,金属性较强的是________(用元素符号表示),下列表述中能证明这一事实的是__________(填序号)。
①Y单质的熔点比Z单质低 ②Y的化合价比Z低
③Y单质与水反应比Z单质剧烈 ④Y最高价氧化物的水化物的碱性比Z强
(4)X元素的气态氢化物与其最高价含氧酸反应的方程式为______________________
(5)元素T和氢元素以原子个数比1∶1化合形成化合物Q,元素X与氢元素以原子个数比1∶2化合形成常用作火箭燃料的化合物W,Q与W发生氧化还原反应,生成X单质和T的另一种氢化物,写出该反应的化学方程式________________________________________