题目内容
【题目】在一个U形管里盛有氯化铜溶液,按如图所示连接。
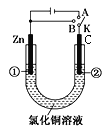
(1)如果把电键K接A,该装置应是________池,Zn是________极; 碳棒电极反应为________________。
(2)上述反应进行5 min后,转换电键K到B,则这一装置是________池,C是________极,Zn的电极反应式是_______________________。
【答案】电解池 阳 Cu2++2e-=Cu 原电池 正 Zn-2e-=Zn2+
【解析】
(1)如果把电键K接A,该装置是电解池,①是阳极、②是阴极,阴极上铜离子放电;
(2)上述反应进行5min后,转换电键K到B,①电极材料是Zn、②电极材料是C和Cu,该装置构成原电池,结合原电池原理分析解答。
(1)如果把电键K接A,该装置是电解池,①是阳极、②是阴极,阴极上铜离子放电,电极反应式为Cu2++2e-=Cu,故答案为:电解池;阳;Cu2++2e-=Cu;
(2)上述反应进行5min后,转换电键K到B,①电极材料是Zn、②电极材料是C和Cu,该装置构成原电池,锌易失电子作负极、②作正极,负极(Zn)的电极反应式为Zn-2e-=Zn2+,故答案为:原电池;正;Zn-2e-=Zn2+。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案【题目】将一定量的SO2(g)和O2(g)分别通入体积为2L的恒容密闭容器中,在不同温度下进行反应,得到如下表中的两组数据:已知2SO2(g)+ O2(g) ![]() 2SO3(g) △H<0
2SO3(g) △H<0
实验 编号 | 温度/℃ | 平衡常数 | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
SO2 | O2 | SO2 | O2 | ||||
1 | T1 | K1 | 4 | 2 | x | 0.8 | 6 |
2 | T2 | K2 | 4 | 2 | 0.4 | y | t |
下列说法中不正确的是( )
A. x=2.4
B. 实验1在前6 min的反应速率v(SO2)=0.2 mol·L-1·min-1
C. K1、K2的关系:K2>K1
D. T1、T2的关系:T1>T2