题目内容
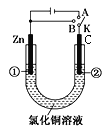
【题目】Ⅰ.某化学兴趣小组为探究铜跟浓硫酸的反应,用如图所示装置进行有关实验。

(1) 装置A中发生反应的化学方程式为___________。
(2) 装置D中试管口放置的棉花应浸一种溶液,这种溶液是______,其作用是___________。
(3) 装置B的作用是贮存多余的气体,当D处有明显的现象后,关闭旋塞K,移去酒精灯, 但由于余热的作用,A处仍有气体产生,此时B中现象是____。
Ⅱ.乙酸乙酯广泛用于药物、染料、香料等工业,甲、乙两同学分别设计如下装置来 制备乙酸乙酯,已知:乙酸乙酯的沸点为77.1℃,CH3CH2OH![]() CH2=CH2↑+H2O。
CH2=CH2↑+H2O。
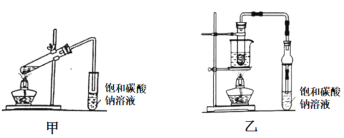
(1)甲装置中右边导管未插入溶液中的目的是 _________。
(2)实验结束后分离出乙酸乙酯的操作是______,必须用到的玻璃仪器有_______(填序号)。
A. 烧杯 B. 容量瓶 C. 分液漏斗 D. 蒸馏烧瓶
(3)乙装置优于甲装置的理由________ (写两条)。
【答案】Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O NaOH 吸收多余的SO2 瓶中液面下降,漏斗液面上升 防倒吸 分液 AC 加热受热均匀、便于控制温度;原料损失较少;不易发生副反应;干燥管下端插入液面,能更好吸收乙酸乙酯。(写两条)
CuSO4+SO2↑+2H2O NaOH 吸收多余的SO2 瓶中液面下降,漏斗液面上升 防倒吸 分液 AC 加热受热均匀、便于控制温度;原料损失较少;不易发生副反应;干燥管下端插入液面,能更好吸收乙酸乙酯。(写两条)
【解析】
铜和浓硫酸反应生成硫酸铜、二氧化硫和水,生成二氧化硫能使品红溶液褪色,发生明显现象后关闭活塞K,拆离酒精灯,余热还会继续生成二氧化硫,二氧化硫进入到B中,B中液面下降,漏斗中液面上升。
Ⅰ(1) 装置A中是铜和浓硫酸反应生成硫酸铜、二氧化硫和水,其反应的化学方程式为Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O;故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;故答案为:Cu+2H2SO4(浓) ![]() CuSO4+SO2↑+2H2O。
CuSO4+SO2↑+2H2O。
(2)装置D中试管口放置的棉花应浸一种溶液,由于二氧化硫会污染环境,因此这种溶液是吸收二氧化硫,即溶液为氢氧化钠溶液;故答案为:NaOH;吸收多余的SO2。
(3) 装置B的作用是贮存多余的气体,当D处有明显的现象后,关闭旋塞K,移去酒精灯, 但由于余热的作用,A处仍有气体产生,产生的气体进入到B中,B中液面下降,漏斗中液面上升;故答案为:瓶中液面下降,漏斗液面上升。
Ⅱ(1)甲装置中右边导管未插入溶液中的目的是防倒吸;故答案为:防倒吸。
(2)乙酸乙酯是难溶于水,溶液分层,因此实验结束后分离出乙酸乙酯的操作是分液;必须用到的玻璃仪器有分液漏斗、烧杯;故答案为:分液;AC。
(3)乙装置水浴加热,受热均匀、便于控制温度;原料损失较少;不易发生副反应;干燥管下端插入液面,能更好吸收乙酸乙酯,也便于防倒吸(写两条);故答案为:加热受热均匀、便于控制温度;原料损失较少;不易发生副反应;干燥管下端插入液面,能更好吸收乙酸乙酯(写两条)。

 阅读快车系列答案
阅读快车系列答案