题目内容
3.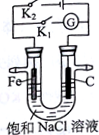 如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中.下列叙述正确的是( )
如图所示,将铁棒和石墨棒插入盛有饱和NaCl溶液的U型管中.下列叙述正确的是( )| A. | K1闭合,向铁棒附近滴入K3[Fe(CN)6]溶液,有蓝色沉淀出现 | |
| B. | K1闭合,电流方向由铁棒经导线流向石墨棒 | |
| C. | K2闭合,碳棒是阴极 | |
| D. | K2闭合,电路中通过0.2NA个电子时,两极共产生4.48L气体 |
分析 若闭合K1,该装置没有外接电源,所以构成了原电池;组成原电池时,较活泼的金属铁作负极,负极上铁失电子发生氧化反应;石墨棒作正极,正极上氧气得电子生成氢氧根离子发生还原反应;若闭合K2,该装置有外接电源,所以构成了电解池,Fe与负极相连为阴极,碳棒与正极相连为阳极,以此解答该题.
解答 解:A.若闭合K1,该装置没有外接电源,所以构成了原电池,较活泼的金属铁作负极,负极上铁失电子,Fe-2e-=Fe2+,则向铁棒附近滴入K3[Fe(CN)6]溶液,有蓝色沉淀出现,故A正确;
B.若闭合K1,该装置没有外接电源,所以构成了原电池;不活泼的石墨棒作正极,电流方向由正极经导线流向铁棒,故B错误;
C.K2闭合,Fe与负极相连为阴极,碳棒为阳极,故C错误;
D.K2闭合,电路中通过0.2NA个电子时,阴极生成0.1mol氢气,阳极生成0.1mol氯气,两极共产生0.2mol气体,但由于气体存在的外界条件未知,则不能确定体积大小,故D错误.
故选A.
点评 本题考查了原电池原理和电解池原理,为高频考点,侧重于学生的分析、计算能力的考查,能正确判断电池的类型及两极的反应是解本题的关键,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.有机物的种类繁多,但其命名是有规则的.下列有机物命名正确的是( )
| A. | CH3CH(CH2CH3)CH2CH3 2-乙基丁烷 | B. | CH2CHBr2 二氯乙烷 | ||
| C. | CH3CH(CH3)CH=CH2 2-甲基丁烯 | D. | 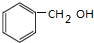 苯甲醇 苯甲醇 |
14.如图所示:2个甲分子反应生成1个丙分子和3个乙分子,对此下列判断不正确的是( )

| A. | 1个乙分子中含有3个A原子 | B. | 该反应类型是分解反应 | ||
| C. | 反应生成的丙物质属于单质 | D. | 化学反应中分子的种类发生了改变 |
18.碱性电池具有容量大、放电电流大的特点,因而得到广泛应用.锌-锰碱性电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)═Zn(OH)2(s)+Mn2O3(s).则下列说法正确的是( )
| A. | .电池工作时,MnO2发生还原反应 | |
| B. | .电池负极的电极反应式为:2MnO2+H2O+2e-→Mn2O3+2OH- | |
| C. | .电池工作时,电路中每通过0.2mol电子,锌的质量理论上减少6.5g | |
| D. | 电池工作时,K+移向负极 |
8.工业上,下列金属冶炼需要采用电解法的是( )
| A. | Ag | B. | Cu | C. | Fe | D. | Mg |
15.设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol 甲基(-CH3)中含有的电子总数为NA | |
| B. | 标准状况下,11.2 L乙醇所含碳原子数目为NA | |
| C. | 常温常压下,26 g 苯中所含的碳碳双键数为NA | |
| D. | 23g钠在足量氧气充分燃烧,转移电子数为NA |
12.已知鲨烯分子含有30个C原子及6个C=C且不含环状结构,则其分子式为( )
| A. | C30H50 | B. | C30H52 | C. | C30H56 | D. | C30H60 |