题目内容
反应,最简单的Diels-Alder反应是共轭双烯与含烯键或炔键的化合物相互作用生成六元环状化合物的 .
.
氯丁橡胶是理想的电线电缆材料,其单体2-氯-1,3-丁二烯也是一种重要的有机合成中间体,该单体的一种合成路线及有关转化关系图如图.
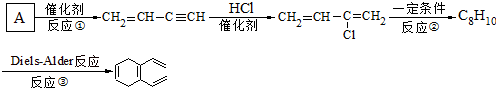
已知:CH2=CH-C≡CH由A二聚得到.
(1)A的结构式为 ,反应①的反应类型是 .
(2)A在一定条件下可以四聚成环状化合物C8H8,其结构简式为 .
(3)C8H8的一种同分异构体属于芳香烃,该芳香烃与1,3-丁二烯可以合成丁苯橡胶,写出此合成反应的化学方程式 .
(4)写出反应③的化学方程式 .
(5)2-氯-1,3-丁二烯的另一种制法是由1,3-丁二烯通过两步反应制得,写出有关的化学方程式 .
 .
.氯丁橡胶是理想的电线电缆材料,其单体2-氯-1,3-丁二烯也是一种重要的有机合成中间体,该单体的一种合成路线及有关转化关系图如图.

已知:CH2=CH-C≡CH由A二聚得到.
(1)A的结构式为
(2)A在一定条件下可以四聚成环状化合物C8H8,其结构简式为
(3)C8H8的一种同分异构体属于芳香烃,该芳香烃与1,3-丁二烯可以合成丁苯橡胶,写出此合成反应的化学方程式
(4)写出反应③的化学方程式
(5)2-氯-1,3-丁二烯的另一种制法是由1,3-丁二烯通过两步反应制得,写出有关的化学方程式
考点:有机物的推断
专题:有机物的化学性质及推断
分析:CH2=CH-C≡CH由A二聚得到,应是发生加成反应得到,则A为HC≡CH,CH2=CH-C≡CH与HCl发生加成反应得到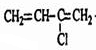 ,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为
,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为 ,
, 和乙炔发生加成反应生成
和乙炔发生加成反应生成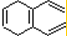 ,再结合题目分析解答.
,再结合题目分析解答.
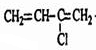 ,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为
,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为 ,
, 和乙炔发生加成反应生成
和乙炔发生加成反应生成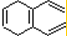 ,再结合题目分析解答.
,再结合题目分析解答.解答:
解:CH2=CH-C≡CH由A二聚得到,应是发生加成反应得到,则A为HC≡CH,CH2=CH-C≡CH与HCl发生加成反应得到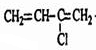 ,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为
,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为 ,
, 和乙炔发生加成反应生成
和乙炔发生加成反应生成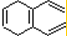 ,
,
(1)利用题中信息H2C=CH-C≡CH由A二聚得到,则A为HC≡CH,反应①的反应类型是加成反应,
故答案为:HC≡CH;加成反应;
(2)A为HC≡CH,在一定条件下可以四聚成环状化合物C8H8,四聚得到的环状产物为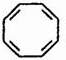 ,
,
故答案为: ;
;
(3)C8H8的一种同分异构体属于芳香烃,该芳香烃与1,3-丁二烯可以合成丁苯橡胶,则该芳香烃为为苯乙烯,合成反应的化学方程式为: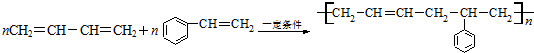 ,
,
故答案为: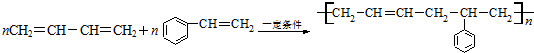 ;
;
(4)反应③的化学方程式为: ,
,
故答案为: ;
;
(5)2-氯-1,3-丁二烯的另一种制法是由1,3-丁二烯通过两步反应制得,第一步为1,3-丁二烯和氯气发生加成反应生成3,4-二氯-1-丁烯,3,4-二氯-1-丁烯和氢氧化钠的醇溶液发生消去反应生成2-氯-1,3-丁二烯,有关的化学方程式为: ,
,
故答案为: .
.
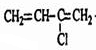 ,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为
,其名称为2-氯-1,3-丁二烯,2-氯-1,3-丁二烯发生反应生成C8H10,根据已知条件知,反应②为消去、加成反应,C8H10的结构简式为 ,
, 和乙炔发生加成反应生成
和乙炔发生加成反应生成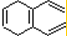 ,
,(1)利用题中信息H2C=CH-C≡CH由A二聚得到,则A为HC≡CH,反应①的反应类型是加成反应,
故答案为:HC≡CH;加成反应;
(2)A为HC≡CH,在一定条件下可以四聚成环状化合物C8H8,四聚得到的环状产物为
 ,
,故答案为:
 ;
;(3)C8H8的一种同分异构体属于芳香烃,该芳香烃与1,3-丁二烯可以合成丁苯橡胶,则该芳香烃为为苯乙烯,合成反应的化学方程式为:
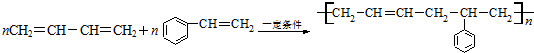 ,
,故答案为:
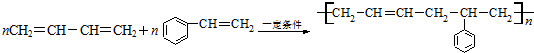 ;
;(4)反应③的化学方程式为:
 ,
,故答案为:
 ;
;(5)2-氯-1,3-丁二烯的另一种制法是由1,3-丁二烯通过两步反应制得,第一步为1,3-丁二烯和氯气发生加成反应生成3,4-二氯-1-丁烯,3,4-二氯-1-丁烯和氢氧化钠的醇溶液发生消去反应生成2-氯-1,3-丁二烯,有关的化学方程式为:
 ,
,故答案为:
 .
.
点评:本题考查了有机物推断,根据有机物中存在的官能团结合题给信息推断有机物,知道发生加成反应时有机物的断键和成键方式,知道发生反应的条件,反应物相同、反应条件不同导致产物不同,题目难度中等.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
下列物质既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
①Ca(OH)2 ②Al2O3 ③Ca(HCO3)2 ④Al(OH)3 ⑤NaHSO4 ⑥Al.
①Ca(OH)2 ②Al2O3 ③Ca(HCO3)2 ④Al(OH)3 ⑤NaHSO4 ⑥Al.
| A、①②④⑥ | B、②③④⑥ |
| C、②③④ | D、②③④⑤⑥ |
下列溶液中一定呈中性的是( )
| A、PH=7的溶液 |
| B、c(H+)=c( OH-)的溶液 |
| C、盐溶液 |
| D、既含有H+ 又含有OH-的溶液 |

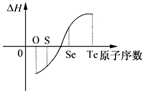 某化学兴趣小组专门研究了氧族元素及其某些化合物的部分性质.所查资料信息如下:
某化学兴趣小组专门研究了氧族元素及其某些化合物的部分性质.所查资料信息如下: