题目内容
现有金属单质A、B和气体甲、乙、丙及物质C、D、E、F,其中B为使用最广泛的金属.它们之间能发生如下反应(图中有些反应的产物和反应的条件没有全部标出).已知:FeCl2可被Cl2氧化为FeCl3

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A 丙
(2)写出下列反应化学方程式:
反应① ;
反应③ ;
(3)写出反应④的离子方程式 .

请根据以上信息回答下列问题:
(1)写出下列物质的化学式:A
(2)写出下列反应化学方程式:
反应①
反应③
(3)写出反应④的离子方程式
考点:无机物的推断,常见金属元素的单质及其化合物的综合应用
专题:推断题,几种重要的金属及其化合物
分析:金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,C为NaOH,黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质D为盐酸.氢氧化钠与物质E反应生成红褐色沉淀是Fe(OH)3,故物质E中含有Fe3+,由转化关系可知,B为Fe,F为FeCl2,E为FeCl3,结合物质的性质解答该题.
解答:
解:金属单质A的焰色反应为黄色,应为Na,与水反应生成的气体甲为H2,C为NaOH,黄绿色气体乙为Cl2,与氢气反应生成丙为HCl,HCl溶于水得物质D为盐酸.氢氧化钠与物质E反应生成红褐色沉淀是Fe(OH)3,故物质E中含有Fe3+,由转化关系可知,B为Fe,F为FeCl2,E为FeCl3,
(1)由以上分析可知,A为Na,丙为HCl,故答案为:Na;HCl;
(2)反应①为钠和水的反应,生成氢氧化钠和氢气,反应的方程式为:2Na+2H2O=2NaOH+H2↑,
反应③是Fe与盐酸反应生成氯化亚铁与氢气,反应的方程式为:Fe+2HCl═FeCl2+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;Fe+2HCl═FeCl2+H2↑;
(3)反应④是氯气与氯化亚铁反应生成氯化铁,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,
故答案为:2Fe2++Cl2═2Fe3++2Cl-.
(1)由以上分析可知,A为Na,丙为HCl,故答案为:Na;HCl;
(2)反应①为钠和水的反应,生成氢氧化钠和氢气,反应的方程式为:2Na+2H2O=2NaOH+H2↑,
反应③是Fe与盐酸反应生成氯化亚铁与氢气,反应的方程式为:Fe+2HCl═FeCl2+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;Fe+2HCl═FeCl2+H2↑;
(3)反应④是氯气与氯化亚铁反应生成氯化铁,反应的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,
故答案为:2Fe2++Cl2═2Fe3++2Cl-.
点评:本题是考查无机物推断,难度中等,掌握元素化合物的性质是解题的关键,需要学生熟练掌握元素化合物知识,注意特殊的颜色与特殊反应是推断的突破口.

练习册系列答案
 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
利用如图装置可实现在铜片上镀镍,下列有关说法不正确的是( )


| A、a为正极,d极为铜片 |
| B、甲池是燃料电池、乙池是电镀池 |
| C、b极上发生的电极反应为:CH4+10OH--8e-═CO32-+7H2O |
| D、c极上发生的电极反应为:Ni2++2e-═Ni |
常温下,在密闭固定体积容器里分别充入两种气体各0.1mol,在一定条件下充分反应后,恢复到原温度时,压强降低为开始时的
.则原混合气体可能是( )
| 3 |
| 4 |
| A、CO和O2 |
| B、HCl和NH3 |
| C、H2和Cl2 |
| D、H2和O2 |
下列有关胶体的叙述不正确的是( )
| A、胶体粒子直径在1-100nm之间 |
| B、氢氧化铁胶体属于纯净物 |
| C、净水剂在水中形成的分散系是胶体 |
| D、光束通过胶体时有丁达尔效应 |
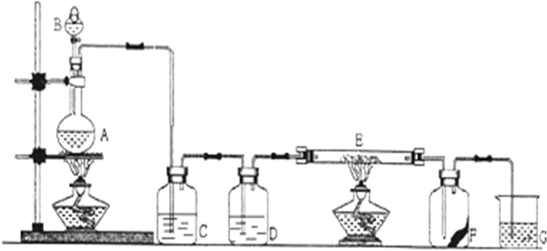
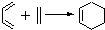 .
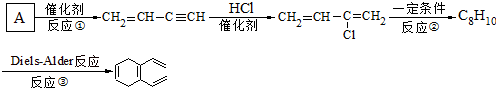
.
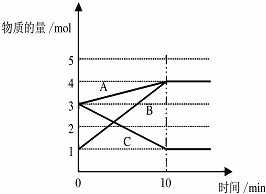 (1)将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如图所示.
(1)将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如图所示.