题目内容
14.下列反应的离子方程式书写错误的是( )| A. | Ca(HCO3)2溶液中加入足量的Ba(OH)2溶液:Ca2++2HCO3-+Ba2++2OH-=CaCO3↓+BaCO3↓+2H2O | |
| B. | 3molCl2通入含2molFeI2的溶液中:2Fe2++4I-+3Cl2=2Fe3++6Cl-+2I2 | |
| C. | 往Ba(OH)2溶液中逐滴加入NH4Al(SO4)2溶液,可能发生反应的离子方程式是Al3++SO42-+Ba2++3OH-=BaSO4↓+Al(OH)3↓ | |
| D. | 向苯酚钠溶液中通入少量的CO2: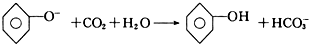 |
分析 A.氢氧化钡足量反应生成碳酸钙、碳酸钡和水;
B.碘离子还原性强于二价铁离子,氯气先氧化碘离子再氧化二价铁离子;
C.Ba(OH)2足量,硫酸根离子生成硫酸钡、氨根离子生成一水合氨,铝离子生成偏铝酸根离子;
D.苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠.
解答 解:A.Ca(HCO3)2溶液中加入足量的Ba(OH)2溶液,离子方程式:Ca2++2HCO3-+Ba2++2OH-=CaCO3↓+BaCO3↓+2H2O,故A正确;
B.3molCl2通入含2molFeI2的溶液中,离子方程式:2Fe2++4I-+3Cl2=2Fe3++6Cl-+2I2,故B正确;
C.往Ba(OH)2溶液中逐滴加入NH4Al(SO4)2溶液,反应的离子方程式为:NH4++Al3++2SO42-+2Ba2++5OH-=2BaSO4↓+NH3•H2O+AlO2-+2H2O,故C错误;
D.苯酚钠与二氧化碳反应生成苯酚和碳酸氢钠,离子方程式: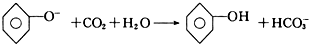 ,故D正确;
,故D正确;
故选:C.
点评 本题考查了离子方程式的书写,把握发生的反应及离子反应的书写方法为解答的关键,侧重与量有关的离子反应考查,注意离子反应的先后顺序为解答的难点,题目难度较大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
4.下列说法中正确的是( )
| A. | 完全由非金属组成的化合物不一定是共价化合物 | |
| B. | 构成分子晶体的粒子一定含有共价键 | |
| C. | 分子晶体的熔点一定比金属晶体的熔点低 | |
| D. | 含有金属离子的晶体一定是离子晶体 |
5.下列实验操作或叙述正确的是( )
| A. | 通过导电实验证明氢氧化铁胶体带正电 | |
| B. | 除去苯中溶有的少量乙醇,加入水,振荡,然后分液 | |
| C. | 进行蒸馏操作时.应用温度计准确测量沸腾液体的温度 | |
| D. | 从海带中提取碘时用到的药品有双氧水和NaOH溶液 |
9.两种气态烃的混合物共2.24L(标准状况),完全燃烧后得3.36L(标准状况)二氧化碳和2.7g的水.下列说法中正确的是( )
| A. | 混合气体中一定含有乙烯 | |
| B. | 混合气体中一定含有甲烷 | |
| C. | 混合气体中一定含有乙炔 | |
| D. | 混合气体一定是由烷烃和烯烃构成的混合物 |
6.1,2,3-三苯基环丙烷的三个苯基可以分布在环丙烷环平面的上下,因此有如下两个异构体: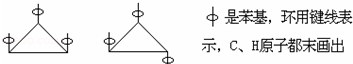
据此,可判断1,2,3,4,5-五氯环戊烷(假定五个碳原子也处于同一平面上)的异构体数目是( )

据此,可判断1,2,3,4,5-五氯环戊烷(假定五个碳原子也处于同一平面上)的异构体数目是( )
| A. | 3 | B. | 4 | C. | 5 | D. | 6 |
4.设NA为阿伏加德罗常数的数值,则下列说法中正确的是( )
| A. | 2.4g金属镁所含电子数目为0.2NA | |
| B. | 1 mol CH4所含质子数目为10NA | |
| C. | 标准状况下22.4 L H2O所含分子数目为NA | |
| D. | 18g NH4+所含电子数目为10NA |
 稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.
稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位.