题目内容
13.硫元素位于元素周期表第16列;硫元素原子核外有2个未成对电子,这2个电子所处亚层的符号是3p;硫、氯元素的原子均可形成与Ar原子电子层结构相同的简单离子,且硫离子的半径更大,请解释氯离子核电荷数更大,对外层电子的引力更强,故离子半径较硫离子小.分析 S的原子序数为16,位于周期表第三周期ⅥA族,原子核外电子排布为1s22s22p63s23p4,核外电子排布相同的离子,核电荷数越大离子半径越小,以此解答.
解答 解:S位于周期表第三周期ⅥA族,位于元素周期表第16列,原子核外电子排布为1s22s22p63s23p4,3p轨道有2个未成对电子,硫、氯元素的原子均可形成与Ar原子电子层结构相同的简单离子,因氯离子核电荷数更大,对外层电子的引力更强,故离子半径较硫离子小,
故答案为:16;3p;氯离子核电荷数更大,对外层电子的引力更强,故离子半径较硫离子小.
点评 本题以硫为载体考查了元素周期律和元素周期表,为高频考点,侧重于学生的分析能力的考查,根据原子结构及元素周期律来分析解答,熟记元素周期律知识,题目难度不大.

练习册系列答案
相关题目
3. 乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)
乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)
填空:
(1)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-;HC2O4-?H++C2O42-,.
(2)KHC2O4溶液显酸性的原因是HC2O4-的电离程度大于水解程度;向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-)
b.c(Na+)=c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-)
d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O;又知该反应开始时速率较慢,随后大大加快,可能的原因是反应生成的Mn2+对该反应具有催化作用.
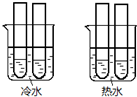
(4)某同学设计实验如图所示:两个烧杯中的试管都分别盛有2mL 0.1 mol/L H2C2O4溶液和4mL 0.1mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对反应速率的影响,但该实验始终没有看到溶液褪色,推测原因KMnO4溶液过量.
(5)已知草酸(H2C2O4)受热分解的化学方程式为:H2C2O4→H2O+CO↑+CO2↑,写出FeC2O4在密闭容器中高温分解的化学方程式FeC2O4$\frac{\underline{\;高温\;}}{\;}$Fe+2CO2↑.
 乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)
乙二酸俗称草酸(结构简式为HOOC-COOH,可简写为H2C2O4),它是一种重要的化工原料.(常温下0.01mol/L的H2C2O4、KHC2O4、K2C2O4溶液的pH如表所示.)| H2C2O4 | KHC2O4 | K2C2O4 | |
| pH | 2.1 | 3.1 | 8.1 |
(1)写出H2C2O4的电离方程式H2C2O4?H++HC2O4-;HC2O4-?H++C2O42-,.
(2)KHC2O4溶液显酸性的原因是HC2O4-的电离程度大于水解程度;向0.1mol/L的草酸氢钾溶液里滴加NaOH溶液至中性,此时溶液里各粒子浓度关系正确的是ad.
a.c(K+)=c(HC2O4-)+c(H2C2O4)+c(C2O42-)
b.c(Na+)=c(H2C2O4)+c(C2O42-)
c.c(K+)+c(Na+)=c(HC2O4-)+c(C2O42-)
d.c(K+)>c(Na+)
(3)H2C2O4与酸性高锰酸钾溶液反应,现象是有气泡(CO2)产生,紫色消失.写出反应的离子方程式2MnO4-+5H2C2O4+6H+→2Mn2++10CO2↑+8H2O;又知该反应开始时速率较慢,随后大大加快,可能的原因是反应生成的Mn2+对该反应具有催化作用.
(4)某同学设计实验如图所示:两个烧杯中的试管都分别盛有2mL 0.1 mol/L H2C2O4溶液和4mL 0.1mol/L 酸性KMnO4溶液,分别混合并振荡,记录溶液褪色所需时间.该实验目的是研究温度对反应速率的影响,但该实验始终没有看到溶液褪色,推测原因KMnO4溶液过量.
(5)已知草酸(H2C2O4)受热分解的化学方程式为:H2C2O4→H2O+CO↑+CO2↑,写出FeC2O4在密闭容器中高温分解的化学方程式FeC2O4$\frac{\underline{\;高温\;}}{\;}$Fe+2CO2↑.
4.X、Y、Z、W为四种短周期元素,它们在周期表中位于连续的四个主族,如图所示.Z元素原子最外层电子数是内层电子总数的$\frac{1}{5}$.下列说法中正确的是( )
| X | Y | ||
| Z | W |
| A. | 原子半径由小到大的顺序为X<Z<Y<W | |
| B. | Y元素最高价氧化物对应的水化物化学式为HYO3 | |
| C. | X、Z两种元素的氧化物中所含化学键类型相同 | |
| D. | Y最简单气态氢化物比Y相邻周期同主族元素气态氢化物沸点高 |
1.稀土元素是指元素周期表中原子序数为57到71的15种镧系元素,以及与镧系元素化学性质相似的钪(Sc)和钇(Y)共17 种元素.回答下列问题;
(1)钪(Sc)元素的原子核外电子排布式为1s22s22p63s23p63d14s2.钬(Ho)的基态原子电子排布式为[Xe]4f116s2,一个基态钛原子所含的未成对电子数为2.
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价.请根据下表中的电离能数据判断表中最有可能有+4价的元素是Ce.
几种稀土元素的电离能(单位:kJ•mol-1)
(3)离子化合物 Na3[Sc(OH)6]中,存在的作用力除离子键外还有共价键和配位键.
(4)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点.则PrO2(二氧化镨)的晶胞中有8个氧原子.
(6)Ce(铈)单质为面心立方晶体,晶胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12,列式表示Ce(铈)单质的密度:$\frac{4×140}{6.02×1{0}^{23}×(516×1{0}^{-10}){\;}^{3}}$g•cm-3(不必计算出结果)
(1)钪(Sc)元素的原子核外电子排布式为1s22s22p63s23p63d14s2.钬(Ho)的基态原子电子排布式为[Xe]4f116s2,一个基态钛原子所含的未成对电子数为2.
(2)稀土元素最常见的化合价为+3价,但也有少数还有+4价.请根据下表中的电离能数据判断表中最有可能有+4价的元素是Ce.
几种稀土元素的电离能(单位:kJ•mol-1)
| 元素 | I1 | I2 | I3 | I1+I2+I3 | I4 |
| Sc(钪) | 633 | 1235 | 2389 | 4257 | 7019 |
| Y(钇) | 616 | 1181 | 1980 | 3777 | 5963 |
| La(镧) | 538 | 1067 | 1850 | 3455 | 4819 |
| Ce(铈) | 527 | 1047 | 1949 | 3523 | 3547 |
(4)Sm(钐)的单质与1,2-二碘乙烷可发生如下反应:Sm+ICH2CH2I→SmI2+CH2=CH2.ICH2CH2I中碳原子杂化轨道类型为sp3,1mol CH2=CH2中含有的σ键数目为5NA.
(5)PrO2(二氧化镨)的晶体结构与CaF2相似,晶胞中Pr(镨)原子位于面心和顶点.则PrO2(二氧化镨)的晶胞中有8个氧原子.
(6)Ce(铈)单质为面心立方晶体,晶胞参数为a=516pm.晶胞中Ce(铈)原子的配位数为12,列式表示Ce(铈)单质的密度:$\frac{4×140}{6.02×1{0}^{23}×(516×1{0}^{-10}){\;}^{3}}$g•cm-3(不必计算出结果)
8.用定量的方法,可用于鉴别邻甲基苯酚和间甲基苯酚的试剂是( )
| A. | 酸性高锰酸钾溶液 | B. | 浓溴水 | ||
| C. | 氯化铁溶液 | D. | 氢氧化钠溶液 |
18.含不溶杂质的NaN03样品,加入一定量蒸馏水使其充分溶解,情况如表:
NaNO3溶解度(g/100g水)如表:
(1)实验中加入的水为300g;
(2)原样品中NaN03为372g.
| 温度(℃) | 10 | 40 | 75 |
| 剩余固体质量(g) | 201 | 132 | 72 |
| 温度(℃) | 10 | 40 | 75 |
| 溶解度 | 81 | 104 | 150 |
(2)原样品中NaN03为372g.
5.常温下,往饱和石灰水中加入一定量的生石灰,一段时间后恢复到原温度,以下叙述错误的是( )
| A. | 有溶质析出 | B. | 溶液中Ca2+的数目不变 | ||
| C. | 溶剂的质量减小 | D. | 溶液的pH不变 |
3.下列关于元素周期律的说法中正确的是( )
| A. | 目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 | |
| B. | 元素的性质随着原子序数的增加而呈周期性变化 | |
| C. | 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 | |
| D. | 可以利用元素周期律预测新元素 |