题目内容
3.下列关于元素周期律的说法中正确的是( )| A. | 目前发现的所有元素占据了周期表里全部位置,不可能再有新的元素被发现 | |
| B. | 元素的性质随着原子序数的增加而呈周期性变化 | |
| C. | 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 | |
| D. | 可以利用元素周期律预测新元素 |
分析 A.元素周期表没有填满,还可以再发现新的元素;
B.原子最外层电子数决定元素的性质;
C.俄国化学家门捷列夫对元素周期表做出了巨大贡献;
D.根据元素在周期表中的位置,结合元素周期律的相似性和递变性,可推知元素可能具有的性质.
解答 解:A.随着科学技术的发展,人们可以不断合成一些元素,元素周期表中元素的种类在不断的增加,故A错误;
B.原子最外层电子数决定元素的性质,元素周期表中元素的核外电子排布呈周期性变化,则元素性质呈周期性变化,故B正确;
C.俄国化学家门捷列夫对元素周期表做出了巨大贡献,而不是道尔顿,故C错误;
D.根据元素在周期表中的位置,结合元素周期律的相似性和递变性,可推知元素可能具有的性质,故D正确,
故选BD.
点评 本题考查元素周期表与元素周期律知识,题目难度不大,注意相关基础知识的积累.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
14.在一定温度下,将足量的AgCl固体分别加入①10mL蒸馏水②30mL0.1mol•L-1NaCl溶液;③5ml 0.5 mol•L-1NaCl溶液; ④10ml 0.2 mol•L-1HCl溶液中.使AgCl溶解并达到饱和,各溶液中Ag+浓度由大到小排列的正确顺序是 ( )
| A. | ④>②>③>① | B. | ①>②>③>④ | C. | ①>②>④>③ | D. | ①>③>②>④ |
11.已知某有机物A的结构简式如下:
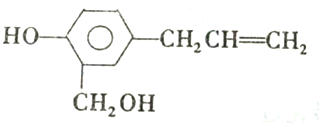 对该物质的性质判断正确的是( )
对该物质的性质判断正确的是( )
 对该物质的性质判断正确的是( )
对该物质的性质判断正确的是( )| A. | 等量A分别与Na和NaOH反应消耗二者的物质的量相同 | |
| B. | 1 mol A 可与2 mol Br2发生取代反应 | |
| C. | A与Na2CO3反应可放出CO2 | |
| D. | 1 mol A 可与4 mol H2发生反应 |
11.下面是实验探究同一主族元素性质的递变规律
(1)探究碱金属从锂到铯金属性的递变规律,通常设计Na、K单质与水反应对比来说明.请描述K与水反应的现象钾迅速熔化成一小球,四处游动,发出轻微爆炸声,有紫色火焰产生,反应的化学方程式为2K+2H2O=2KOH+H2↑,比Na跟水反应更剧烈.
(2)探究卤素从F到I的非金属性的递变规律
某学生设计了如下的实验方案,请帮助该学生整理并完成实验报告.
①实验用品
仪器:试管、胶头滴管
药品:新制的氯水、氯化钠溶液、溴化钠溶液、KI溶液、四氯化碳
②实验内容(在下表留空的格中填写相关内容)
(1)探究碱金属从锂到铯金属性的递变规律,通常设计Na、K单质与水反应对比来说明.请描述K与水反应的现象钾迅速熔化成一小球,四处游动,发出轻微爆炸声,有紫色火焰产生,反应的化学方程式为2K+2H2O=2KOH+H2↑,比Na跟水反应更剧烈.
(2)探究卤素从F到I的非金属性的递变规律
某学生设计了如下的实验方案,请帮助该学生整理并完成实验报告.
①实验用品
仪器:试管、胶头滴管
药品:新制的氯水、氯化钠溶液、溴化钠溶液、KI溶液、四氯化碳
②实验内容(在下表留空的格中填写相关内容)
| 步骤 | 实验方案 | 实验现象(描述最后的) | 离子方程式 |
| ① | 先向试管中加入溴化钠溶液2ml,再加入4-5滴新制氯水,振荡后分两份,取一份又加入CCl4,振荡、静置 | 上层为浅黄色(或无色),下层为橙色 | Cl2+2Br-=Br2+2Cl- |
| ② | 取少量KI溶液于试管,加入几滴步骤①留下的另一份溶液,振荡,又加入CCl4,振荡、静置 | 上层为浅黄色(或无色),下层为紫红色 | Br2+2I-=I2+2Br- |
| 结论 | 氧化性:Cl2>Br2>I2(非金属性:Cl>Br>I) | ||
8.某校化学小组学生利用如图装置进行“氨的催化氧化及检验产物”实验.(图中夹持装置已略去)下列推断合理的是( )
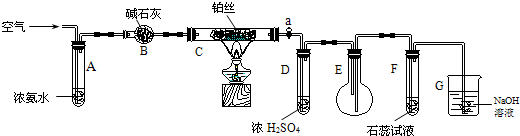

| A. | C不需要持续加热 | |
| B. | D的作用是干燥气体 | |
| C. | B是无用装置 | |
| D. | 仅用该套装置和药品无法达到检验产物的目的 |
9.对物质进行分类是学习化学的一种方法.“冰红茶”“雪碧饮料”“生理盐水”和“矿泉水”均属于( )
| A. | 纯净物 | B. | 混合物 | C. | 氧化物 | D. | 无法判断 |