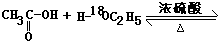题目内容
在学生已经知道氯水的成分后,老师在课堂上演示了一个趣味实验:把一朵带露的红玫瑰放到盛有干燥氯气的集气瓶中.红玫瑰很快变成“白”玫瑰.学生对此进行了猜测.
猜测一:氯气具有漂白性,能使红玫瑰褪色
猜测二:氯气与玫瑰上的水分作用,产生的盐酸使红玫瑰褪色
(1)你认为哪种猜测是正确的?如果你不同意以上两种猜测,请给出你的猜测. .
(2)请你设计实验方案,证明你的观点.(提供的实验用品有:带露的玫瑰、风干的玫瑰、盐酸、干燥的氯气、氯水、蒸馏水,实验仪器自选.)
实验方案: .
猜测一:氯气具有漂白性,能使红玫瑰褪色
猜测二:氯气与玫瑰上的水分作用,产生的盐酸使红玫瑰褪色
(1)你认为哪种猜测是正确的?如果你不同意以上两种猜测,请给出你的猜测.
(2)请你设计实验方案,证明你的观点.(提供的实验用品有:带露的玫瑰、风干的玫瑰、盐酸、干燥的氯气、氯水、蒸馏水,实验仪器自选.)
实验方案:
考点:氯气的化学性质,探究氯水、氯气的漂白作用
专题:实验设计题,元素及其化合物
分析:(1)氯气与水反应生成盐酸、次氯酸和水,次氯酸具有强氧化性能够使有色物质褪色,具有漂白性,据此分析解答;
(2)要证明次氯酸具有漂白性,只需要证明干燥的氯气和盐酸不具有漂白性就行.
(2)要证明次氯酸具有漂白性,只需要证明干燥的氯气和盐酸不具有漂白性就行.
解答:
解:把一朵带露的红玫瑰放到盛有干燥氯气的集气瓶中.红玫瑰很快变成“白”玫瑰.说明玫瑰被漂白了,从反应物和生成物分析应该有三种可能:
一:氯气具有漂白性;
二:盐酸具有漂白性;
三:次氯酸具有漂白性;
我认为:猜测一和二都不正确,应该是氯气与玫瑰上的水分作用生成的另一种物质(次氯酸)使红玫瑰褪色;
故答案为:都不正确 是氯气与玫瑰上的水分作用生成的另一种物质(次氯酸)使红玫瑰褪色;
(2)要证明次氯酸具有漂白性,只需要证明干燥的氯气和盐酸不具有漂白性就行,所以设计实验如下:
将风干的玫瑰放到盛有干燥氯气的集气瓶,红玫瑰不褪色,滴几滴蒸馏水在花瓣上,红玫瑰很快变成“白”玫瑰,说明猜测一是错误的,而且褪色和氯气与水反应产物有关;另取带露的玫瑰放入盛有盐酸的烧杯,红玫瑰不褪色,说明猜测二也是错误的;结合分析两实验,说明是次氯酸使红玫瑰褪色;
故答案为:将风干的玫瑰放到盛有干燥氯气的集气瓶,红玫瑰不褪色,滴几滴蒸馏水在花瓣上,红玫瑰很快变成“白”玫瑰,说明猜测一是错误的,而且褪色和氯气与水反应产物有关;另取带露的玫瑰放入盛有盐酸的烧杯,红玫瑰不褪色,说明猜测二也是错误的;结合分析两实验,说明是次氯酸使红玫瑰褪色.
一:氯气具有漂白性;
二:盐酸具有漂白性;
三:次氯酸具有漂白性;
我认为:猜测一和二都不正确,应该是氯气与玫瑰上的水分作用生成的另一种物质(次氯酸)使红玫瑰褪色;
故答案为:都不正确 是氯气与玫瑰上的水分作用生成的另一种物质(次氯酸)使红玫瑰褪色;
(2)要证明次氯酸具有漂白性,只需要证明干燥的氯气和盐酸不具有漂白性就行,所以设计实验如下:
将风干的玫瑰放到盛有干燥氯气的集气瓶,红玫瑰不褪色,滴几滴蒸馏水在花瓣上,红玫瑰很快变成“白”玫瑰,说明猜测一是错误的,而且褪色和氯气与水反应产物有关;另取带露的玫瑰放入盛有盐酸的烧杯,红玫瑰不褪色,说明猜测二也是错误的;结合分析两实验,说明是次氯酸使红玫瑰褪色;
故答案为:将风干的玫瑰放到盛有干燥氯气的集气瓶,红玫瑰不褪色,滴几滴蒸馏水在花瓣上,红玫瑰很快变成“白”玫瑰,说明猜测一是错误的,而且褪色和氯气与水反应产物有关;另取带露的玫瑰放入盛有盐酸的烧杯,红玫瑰不褪色,说明猜测二也是错误的;结合分析两实验,说明是次氯酸使红玫瑰褪色.
点评:本题属于实验题,考查学生分析、设计实验的能力,题目难度中等,明确氯气和次氯酸的性质是解题关键,注意实验设计的严密性.

练习册系列答案
相关题目
下列各组物质中属于同分异构体的是( )
| A、正丁烷和异丁烷 |
| B、金刚石和石墨 |
| C、12C和13C |
| D、乙烯和乙烷 |
用浓度为0.5mol/L的醋酸与锌反应,若先向该醋酸溶液中加入较多的醋酸钠固体,则产生H2的速率将( )
| A、变快 | B、变慢 |
| C、先变快,后变慢 | D、不变 |
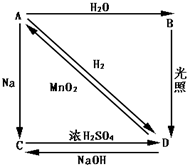 常温下,A是双原子分子气态单质,其密度为3.17g/L(标准状况下),B、C、D都是含A元素的化合物,转化关系如图所示
常温下,A是双原子分子气态单质,其密度为3.17g/L(标准状况下),B、C、D都是含A元素的化合物,转化关系如图所示