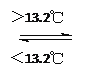题目内容
【题目】在25℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ,下列热化学方程式书写正确的是()
A. CH3OH(l)+3/2O2(g)![]() CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
CO2(g)+2H2O(l) ΔH=+725.76 kJ·mol-1
B. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-1 451.52 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-1 451.52 kJ·mol-1
C. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
2CO2(g)+4H2O(l) ΔH=-725.76 kJ·mol-1
D. 2CH3OH(l)+3O2(g)![]() 2CO2(g)+4H2O(l)ΔH=+1451.52 kJ·mol-1
2CO2(g)+4H2O(l)ΔH=+1451.52 kJ·mol-1
【答案】B
【解析】
1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1451.52 kJ
A、甲醇燃烧是放热反应,焓变值为负值,故A错误;
B、1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1451.52 kJ,热化学方程式为:2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1451.52 kJ·mol-1,故B正确;
C、1g甲醇燃烧生成CO2和液态水时放热22.68 kJ,则64g即2mol甲醇燃烧放的热量为1451.52 kJ,反应热数值计算错误,故C错误;
D、甲醇燃烧是放热反应,焓变值为负值,故D错误。
综上所述,本题正确答案为B。

 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案【题目】在1.0 L真空密闭容器中充入4.0 mol A(g)和4.0 mol B(g),在一定温度下进行反应:A(g)+B(g)![]() C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表:
C(g) ΔH,测得不同时刻该容器内物质的物质的量如下表:
时间/min | 0 | 10 | 20 | 30 | 40 |
n(A)/mol | 4.0 | 2.5 | 1.5 | n2 | n3 |
n(C)/mol | 0 | 1.5 | n1 | 3 | 3 |
回答下列问题:
(1)随着温度的升高,该反应的化学平衡常数减小,则ΔH__________(填“>”“<”或“=”)0,反应从起始到20 min内C的平均反应速率是________。
(2)该温度下,上述反应的化学平衡常数为________。平衡时体系内气体的总压强是反应起始时总压强的________。
(3)下列选项中能说明该反应在一定温度和恒容条件下达到平衡状态的是________。
A.反应速率:vA(正)+vB(正)=vC(逆)
B.A的质量不再改变
C.B的转化率不再改变
D.密度不再改变
(4)若反应C(g)![]() A(g)+B(g) ΔH>0,进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。
A(g)+B(g) ΔH>0,进行时需加入稀释剂X气体(不参与反应),则C的平衡转化率与体系的温度、压强、X的物质的量的关系如图1、图2所示。


①由图1可知,T1________(填“>”“<”或“=”)T2。
②由图2可知,当其他条件不变时,增大X的物质的量,C的平衡转化率将________(填“增大”“减小”或“不变”),其原因是________________。