题目内容
【题目】CO、CO2是含碳元素的常见气体,也是参与碳循环的重要物质。研究和深度开发CO、CO2的应用对构建生态文明社会具有重要的意义。
(1)CO可用于炼铁,已知:
Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0 kJ·mol-1;
C(s) +CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为______________________________。
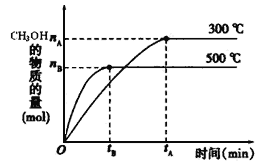
(2)甲醇是重要的化工原料,利用煤化工中生产的CO和H2可制取甲醇,发生的反应为CO(g)+2H2(g) ![]() CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1 mol CO和2 mol H2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
CH3OH(g)。实验室中,在1L恒容的密闭容器中进行模拟合成实验。将1 mol CO和2 mol H2通入容器中,分别恒温在300℃和500℃反应,每隔一段时间测得容器内CH3OH的浓度如下表所示:
10min | 20min | 30min | 40min | 50min | 60min | |
300 ℃ | 0.40 | 0.60 | 0.75 | 0.84 | 0.90 | 0.90 |
500 ℃ | 0.60 | 0.75 | 0.78 | 0.80 | 0.80 | 0.80 |
①300℃和500℃对应的平衡常数大小关系为K300℃_________K500℃(填“>”、“=”或“<”)。
②下列关于该反应的说法正确的是______________(填选项字母,下同)
A.该反应在任何温度下都能自发进行
B.升高温度,正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
C.温度一定时,压强不再随时间变化可以说明反应达到了平衡状态
D.使用高效催化剂,ΔH会增大
③300 ℃时,前10 min内,该反应的平均反应速率为v(H2)=___mol/(L·min)。
④下列措施能够增大此反应中CO的转化率的是_________。
A. 充入CO气体 B. 升高温度
C. 使用优质催化剂 D. 往容器中再充入1 mol CO和2 mol H2
⑤500 ℃时,保持反应体系的温度不变,60min时再向容器中充入CH3OH气体和H2各0.4mol,反应将向___(填“正反应方向”、“逆反应方向”或“不”)进行。再次达到平衡时的平衡常数为____________L2/mol2。
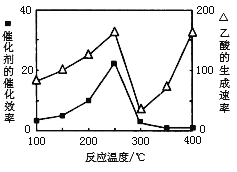
(3)以TiO2/Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率的关系见下图。当乙酸的生成速率主要取决于温度时,其影响范围是__________________。
【答案】Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) △H =-28.5kJ·mol—1 > C 0.08 D 正反应方向 25 300℃~400℃
【解析】
根据盖斯定律计算热化学方程式中的反应热。根据外界条件对反应速率和平衡的影响分析一氧化碳的转化率的变化。根据某时刻的浓度商和平衡常数的比较分析该时刻的进行方向。
(1) ① Fe2O3(s) + 3C(s)=2Fe(s) + 3CO(g) ΔH1=+489.0 kJ·mol-1;②C(s) +CO2(g)=2CO(g) ΔH2=+172.5 kJ·mol-1,根据盖斯定律分析,有①-②×3得热化学方程式为: Fe2O3(s)+ 3CO(g)=2Fe(s)+ 3CO2(g) △H =+489.0kJ/mol-172.5kJ/mol×3=-28.5kJ·mol—1 。
(2) ①从表中数据分析,温度升高,甲醇平衡物质的量浓度减小,说明升温平衡逆向移动,则平衡常数变小 ;
②A.该反应为放热反应,熵减,所以该反应在低温下能自发进行,故错误;B.升高温度,正反应速率和逆反应速率都增大,平衡向逆反应方向移动,故错误;C.温度一定时,压强不再随时间变化说明气体总物质的量不变,可以说明反应达到了平衡状态,故正确;D.使用高效催化剂,不影响反应热,故ΔH不会改变,故错误。故选C;
③300 ℃时,前10 min内,该反应的平均反应速率为v(CH3OH)=0.40mol/L/10min=0.04 mol/(L·min),根据化学计量数计算v(H2)=0.08 mol/(L·min)。
④A. 充入CO气体,平衡正向移动,但一氧化氮的转化率不能提高,故错误;B. 升高温度,平衡逆向移动,一氧化碳的转化率不能提高,故错误;C. 使用优质催化剂不影响平衡,故错误;D. 往容器中再充入1 mol CO和2 mol H2,相当于加压,平衡正向移动,提高一氧化碳的转化率,故正确。故选D。
⑤500 ℃时,
CO(g)+2H2(g) ![]() CH3OH(g)
CH3OH(g)
起始浓度 1 2 0
改变浓度 0.8 1.6 0.8
平衡浓度 0.2 0.4 0.8
平衡常数= ![]() ,保持反应体系的温度不变,60min时再向容器中充入CH3OH气体和H2各0.4mol,Qc=
,保持反应体系的温度不变,60min时再向容器中充入CH3OH气体和H2各0.4mol,Qc= ![]() <K,则反应向正反应方向进行。再次达到平衡,平衡常数不变,为25。
<K,则反应向正反应方向进行。再次达到平衡,平衡常数不变,为25。
(3)从图分析,在 300℃~400℃,温度升高,乙酸的生成速率加快,但催化剂的催化效率降低,说明此阶段中乙酸的生成速率主要取决于温度,故答案为300℃~400℃。

【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO![]() 2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2。为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/(10-4mol·L-1) | 10 | 4.5 | 2.5 | 1.5 | 1.0 | 1.0 |
c(CO)/(10-3mol·L-1) | 36.0 | 30.5 | 28.5 | 27.5 | 27.0 | 27.0 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1) 已知该反应ΔS<0,在上述条件下反应能够自发进行,则反应的ΔH________0(填写“>”“<”或“=”)。
(2)前2 s内的平均反应速率v(N2)=________。
(3)在该温度下,反应的平衡常数表达式K=________。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是________。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
【题目】亚硝酰氯(NOCl,熔点:-64.5 ℃,沸点:-5.5 ℃)是一种黄色气体,遇水易反应生成一种无氧酸和两种氮的常见氧化物。亚硝酰氯应用广泛,可用于合成清洁剂、触媒剂及中间体等。实验室可由氯气与一氧化氮在常温常压下合成。
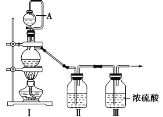
(1)甲组同学拟制备原料气NO和Cl2,制备装置如图所示,为制备纯净干燥的气体,补充右表中缺少的药品。
装置Ⅰ | 装置Ⅱ | ||
蒸馏烧瓶中 | A仪器中 | ||
制备纯净的Cl2 | MnO2 | ①______ | ②______ |
制备纯净的NO | Cu | ③______ | ④______ |
(2)乙组同学对甲组同学制取NO的装置略加改良,结合甲组制得的Cl2共同制备NOCl,装置如图所示:
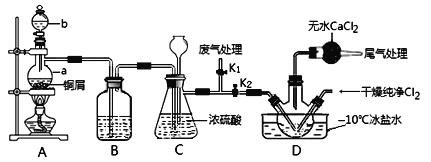
①仪器b的名称为________________。
②组装好实验装置后应先______________,然后依次装入药品。此实验关键操作有两点:一是将Cl2充满D装置的三颈瓶中;二是A中反应开始时要先关闭K2,打开K1,待NO充满装置后再关闭K1,打开K2。这两步操作中充满的目的都是__________________________________________________。
③若C装置中压强过大,可以观察到的现象是_________________________。
④装置D中冰盐水的作用是__________________。
(3)亚硝酰氯(NOCl)纯度的测定:将所得亚硝酰氯(NOCl)产品13.10g溶于水,配制成250mL溶液;取出25.00mL,以K2CrO4溶液为指示剂,用0.8mol·L-1AgNO3标准溶液滴定至终点,消耗标准溶液的体积为 22.50mL。(已知:Ag2CrO4为砖红色固体)
①亚硝酰氯(NOCl)与水反应的化学方程式为_________________________。
②亚硝酰氯(NOCl)的质量分数为______________________。