题目内容
5.下列说法中正确的是( )| A. | 原子及其离子的核外电子层数等于该元素所在的周期数 | |
| B. | 元素周期表中从IIIB族到IIB族 10个纵行的元素都是金属元素 | |
| C. | 第ⅠA族元素的金属性比第ⅡA族元素的金属性强 | |
| D. | 在周期表里,主族元素所在的族序数等于原子核外电子数 |
分析 A、根据钾离子或钠离子等微粒的核外电子层数以及该元素所在的周期数来回答;
B、根据元素周期表中过渡元素的分布来回答;
C、同周期第ⅠA族元素的金属性比第ⅡA族元素的金属性强;
D、主族元素所在的族序数等于最外层电子数.
解答 解:A、钾离子的核外电子层数为3,该元素所在的周期数为4;钠离子的核外电子层数为2,该元素所在的周期数为3,均不相等,故A错误;
B、元素周期表中从IIIB族到IIB族10个纵行的元素都是过渡元素,过渡元素全部为金属元素,故B正确;
C、同周期第ⅠA族元素金属性比第ⅡA族元素强,但不同周期比较,如Na(ⅠA)、Ca(ⅡA),前者金属性较弱,故C错误;
D、主族元素所在的族序数等于最外层电子数,不是核外电子数,故D错误;
故选B.
点评 本题考查学生同主族元素性质的递变规律,可以根据所学知识来回答,难度不大.

练习册系列答案
相关题目
9.能在水溶液中大量共存的一组离子是( )
| A. | Fe2+、Mg2+、SO42-、NO3- | B. | Na+、Ag+、Br-、PO43- | ||
| C. | Ba2+、K+、SO32-、ClO- | D. | Al3+、NH4+、CO32-、Cl- |
13.某有机物的结构简式为 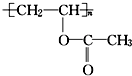 ,下列关于该有机物叙述不正确的是( )
,下列关于该有机物叙述不正确的是( )
 ,下列关于该有机物叙述不正确的是( )
,下列关于该有机物叙述不正确的是( )| A. | 1 mol 该有机物与 NaOH 溶液完全反应时,消耗 NaOH 1 mol | |
| B. | 该有机物水解所得产物能发生取代反应 | |
| C. | 该有机物可通过加聚反应生成 | |
| D. | 该有机物分子中含有双键 |
20.下列关于两种有机化合物A和B的说法中错误的是( )
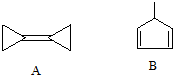

| A. | A的化学式为C6H8 | B. | A的二氯取代产物有4种 | ||
| C. | A与B与溴水反应产物都只有一种 | D. | A分子所有碳原子均在同一平面上 |
10.若从溴水中把溴萃取出来,可选用的萃取剂是( )
| A. | 水 | B. | 无水酒精 | C. | 四氯化碳 | D. | 氢氧化钠溶液 |
17.下列各组离子能大量共存的是( )?
| A. | K+、NH4+、SO42-、NO3- | B. | OH-、K+、NH4+、Cl- | ||
| C. | Fe3+、Cl-、Na+、OH- | D. | Fe2+、H+、SO32-、NO3- |
14.对于以下反应:A(s)+3B(g)?2C(g)+D(g),在一定温度和容积固定的容器中,下列判断正确的是( )
| A. | 若反应是放热反应,升高温度,正反应速率增大 | |
| B. | 往容器中通入稀有气体He,由于压强增大,所以反应速率增大 | |
| C. | 往容器中加入少量A,反应速率增大 | |
| D. | 当容器内的压强不再变化,可以判断反应已经达到平衡 |
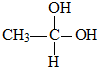 →CH3-CHO+H2O
→CH3-CHO+H2O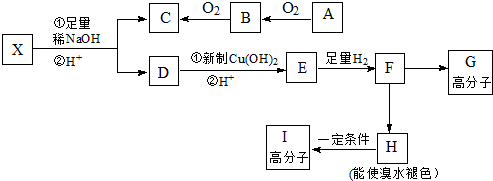
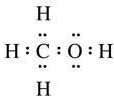 .
. ;
;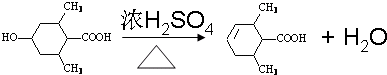 ;
;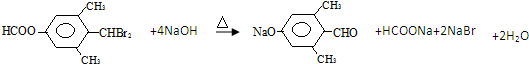 ;
;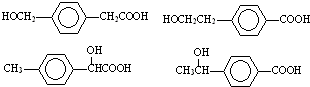 任意一种.
任意一种.