题目内容
13.有关甲、乙两种非金属的下列说法中,能说明甲比乙的非金属性强的是( )①甲与氢气化合比乙容易
②甲的最高价氧化物对应水化物酸性比乙的强
③甲的单质能与乙的阴离子发生置换反应
④甲的氢化物比乙的稳定
⑤甲的氢化物还原性比乙的强
⑥与金属反应甲得电子比乙多.
| A. | ①②③ | B. | ①②③④ | C. | ①②③④⑤ | D. | ①②③④⑤⑥ |
分析 判断非金属性强弱方法有:元素的非金属性越强,其最高价氧化物的水化物酸性越强、其氢化物的稳定性越强、与氢气反应越容易、其氢化物的还原性越弱、其单质的氧化性越强,据此分析解答.
解答 解:判断非金属性强弱方法有:元素的非金属性越强,其最高价氧化物的水化物酸性越强、其氢化物的稳定性越强、与氢气反应越容易、其氢化物的还原性越弱、其单质的氧化性越强,
①甲与氢气化合比乙容易,说明甲的非金属性比乙强,故正确;
②甲的最高价氧化物对应水化物酸性比乙的强,说明甲的非金属性比乙强,故正确;
③甲的单质能与乙的阴离子发生置换反应,则甲单质的氧化性大于乙,所以说明甲的非金属性比乙强,故正确;
④甲的氢化物比乙的稳定,说明甲的非金属性比乙强,故正确;
⑤甲的氢化物还原性比乙的强,说明甲的非金属性比乙弱,故错误;
⑥与金属反应甲得电子比乙多不能说明甲的非金属性大于乙,故错误;
故选B.
点评 本题考查非金属性强弱判断,明确非金属性强弱判断方法是解本题关键,注意不能根据得失电子多少判断非金属性强弱,要根据得电子难易程度判断,题目难度不大.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
3.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 常温常压下,28gCH2=CH2含有NA个碳原子 | |
| B. | 1mol苯含有3NA个碳碳单键和3NA个碳碳双键 | |
| C. | 标准状况下,22.4L正戊烷含有12NA个氢原子 | |
| D. | 常温常压下,16gCH4含有4NA个共价键 |
4.关于结构简式为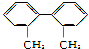 的烃的下列说法正确的是( )
的烃的下列说法正确的是( )
 的烃的下列说法正确的是( )
的烃的下列说法正确的是( )| A. | 分子中至少有6个碳原子共平面 | B. | 分子中至少有8个碳原子共平面 | ||
| C. | 分子中至少有9个碳原子共平面 | D. | 分子中至少有14个碳原子共平面 |
1.下列有关化学用语表示正确的是( )
| A. | CO2的结构式O-C-O | |
| B. | S2-的结构示意图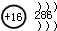 | |
| C. | N2的电子式为  | |
| D. | 质子数为53,中子数为78的碘原子${\;}_{53}^{78}$I |
8.W、X、Y、Z四种短周期元素在周期表中的位置如图所示,W的气态氢化物可与其最高价氧化物对应水化物反应生成离子化合物,由此可知( )
| W | X | |
| Y | Z |
| A. | Z元素的氧化物对应水化物的酸性一定强于Y | |
| B. | X、Y、Z中最简单氢化物稳定性最弱的是Y | |
| C. | X元素的简单离子还原性大于Y | |
| D. | Z元素单质在化学反应中只表现氧化性 |
18.下列属于同分异构体的一组是( )
| A. | 35Cl和37Cl | B. | 白磷和红磷 | ||
| C. | H2O和 D2O | D. | 氰酸铵(NH4OCN)与尿素[CO(NH2)2] |
5.下列分子中,键的极性最强的是( )
| A. | PH3 | B. | H2S | C. | HBr | D. | HCl |
2.有机物A的结构简式如图,下列关于A的性质叙述中,错误的是( )


| A. | 不能发生水解反应 | |
| B. | A能与碳酸钠溶液反应 | |
| C. | A既能与羧酸反应,又能与醇反应 | |
| D. | A与氢氧化钠溶液完全反应时,两者物质的量之比是1:3 |
3.下列说法中,错误的是( )
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 煤、石油、天然气是当今世界最重要的三种化石燃料 | |
| C. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| D. | 化学反应中能量变化的大小与反应物的质量多少无关 |