题目内容
【题目】一种有机物的结构简式如图,关于它的性质不正确的说法是( ) 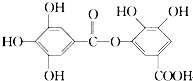
A.它有酸性,1 mol该物质最多能与6 mol H2发生加成反应
B.在一定条件下,1 mol该物质最多能和4 mol Br2反应
C.它可以水解,水解产物为两种有机物
D.该有机物能发生取代反应
【答案】C
【解析】解:A.酚﹣OH、﹣COOH具有酸性,只有苯环与氢气发生加成反应,则1 mol该物质最多能与6 mol H2发生加成反应,故A正确;
B.酚﹣OH的邻、对位与溴水发生取代反应,则在一定条件下,1 mol该物质最多能和4 mol Br2反应,故B正确;
C.含﹣COOC﹣,可发生水解反应,且水解产物只有一种(苯环上3个﹣OH相连,﹣COOH与中间的﹣OH相对),故C错误;
D.含﹣OH、﹣COOH、﹣COOC﹣均可发生取代反应,故D正确;
故选C.
由结构可知,分子中含酚﹣OH、﹣COOC、﹣COOH,结合酚、酯、羧酸的性质来解答.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目