题目内容
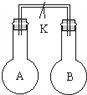
【题目】如图所示,室温时甲、乙两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下止水夹K,使两瓶内气体充分接触后,容器内压强最小的是( )
编号 | A | B | C | D |
甲中气体 | H2S | H2 | NH3 | NO |
乙中气体 | SO2 | Cl2 | HCl | O2 |
A. A B. B C. C D. D
【答案】C
【解析】同温同压时,体积相等的A、B两种气体它们的物质的量相等,为了便于讨论,设气体各有1mol。A、H2S遇到SO2发生反应2H2S+SO2=2H2O+3S,室温时水是液体,S是固体,剩余气体为0.5mol SO2。B、常温下H2与Cl2不发生反应,剩余气体2mol。C、NH3+HCl=NH4Cl,常温时NH4Cl为固体,反应后剩余气体0 mol。D、2NO+O2=2NO2,NO2是气体,反应后剩余气体1.5mol。综上所述,剩余气体最少的是C,容器内压强也最小。正确答案C。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目