题目内容
18.对于HCl、H2SO4、NaOH、NaCl、NH4Cl、Ne、N2、金刚石,回答下列问题:(1)不存在化学键的是Ne.
(2)属于共价化合物的是HCl、H2SO4.
(3)属于离子化合物的是NaOH、NaCl、NH4Cl.
(4)既含离子键,又含共价键的是NH4Cl.
分析 一般活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,氯化铵为离子晶体,由氨根离子与氯离子通过离子键结合在一起;含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物;稀有气体为单原子分子,不存在化学键.
解答 解:(1)稀有气体为单原子分子,不存在化学键,则不存在化学键的是Ne;故答案为:Ne;
(2)非金属元素之间易形成共价键,只含共价键的化合物是共价化合物,则属于共价化合物的是HCl、H2SO4;故答案为:HCl、H2SO4;
(3)一般活泼金属和活泼非金属元素之间易形成离子键,铵盐中存在离子键,则属于离子化合物的是NaOH、NaCl、NH4Cl;
故答案为:NaOH、NaCl、NH4Cl;
(4)氯化铵为离子晶体,由氨根离子与氯离子通过离子键结合在一起,N元素与H元素之间存在共价键,则NH4Cl既含离子键,又含共价键;故答案为:NH4Cl.
点评 本题考查了化学键和化合物的判断,根据物质的构成微粒及微粒间的作用力来分析解答,题目难度不大.

练习册系列答案
相关题目
8.下列对相应微粒的描述中,不正确的是( )
| A. | 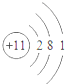 易形成阳离子 | B. | 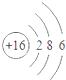 易得电子 | C. |  为稳定结构 | D. | 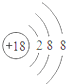 稀有气体的原子 |
13.溶液可能存在电离平衡、水解平衡和溶解平衡等动态平衡.下列说法中正确的是( )
| A. | 25℃时,HClO溶液加水稀释,电离程度增大,溶液中H+浓度增大 | |
| B. | 等物质的量浓度的氨水和盐酸等体积混合,存在:2c(NH4+)+c(H+)+c(NH3•H2O)=2c(Cl-)+c(OH-) | |
| C. | MgCl2饱和溶液蒸干可以得到MgCl2•6H2O,继续灼烧得到无水MgCl2 | |
| D. | 已知Ksp(AgCl)=1.8×10-10(mol/L)2,Ksp(Ag2CrO4)=1.8×10-10(mol/L)3,则Ag2CrO4的溶解度小于AgCl |
11.有机物A的分子式为C6H12O3,一定条件下,A与碳酸氢钠、钠均能产生气体,且生成的气体体积比(同温同压)为1:1,则A的结构最多有( )
| A. | 33种 | B. | 31种 | C. | 28种 | D. | 19种 |
8.下列关系正确的是( )
| A. | 含氢量:苯>乙烯>甲烷 | |
| B. | 密度:H2O>溴苯> | |
| C. | 沸点:戊烷>2-甲基丁烷>2,2-二甲基丙烷 | |
| D. | 等质量的下列物质燃烧耗O2量:乙炔>乙烯>乙烷 |
9.根据有机化合物的命名规则,下列命名正确的是( )
| A. | 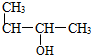 1-甲基-2-丙醇 | B. | 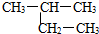 2-甲基丁烷 | C. |  1,2,3-甲基丙烷 | D. | 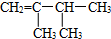 2,3-甲基-3-丁烯 |
 ,写出HFO的结构式H-O-F.
,写出HFO的结构式H-O-F.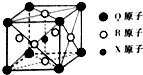 已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大.X基态原子的核外电子分布在3个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和.另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,请回答下列问题.
已知元素X、Y、Z、W、Q均为短周期元素,原子序数依次增大.X基态原子的核外电子分布在3个能级,且各能级电子数相等,Z是地壳中含量最多的元素,W是电负性最大的元素,元素Q的核电荷数等于Y、W原子的最外层电子数之和.另有R元素位于元素周期表第4周期第Ⅷ族,外围电子层有2个未成对电子,请回答下列问题.