题目内容
【题目】(1)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g)2NH3(g)△H。有关键能数据如下:
化学键 | H-H | N-H | N≡N |
键能)kJ/mol) | 436 | 391 | 945 |
根据表中所列键能数据可得△H=____________。
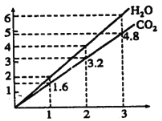
(2)已知:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H= +49.0kJ/mol
CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
已知水的气化热为44.0kJ/mol,表示氢气燃烧热的热化学方程式为______________。
(3)已知化学反应A(g)+B(g)C(g)+D(g),900℃时向一个体积为2L的密闭容器中充入0.20mol A和0.80mol B,2s时达到平衡,A的浓度变化0.05mol/L,则A的平均反应速率v(A) =________,平衡时B的转化率为____ ,C的体积百分数为_______ 。
(4)CO、H2可用于合成甲醇和甲醚,其反应为(m、n均大于![]() ):
):
反应①:CO(g)+2H2(g)CH3OH(g)△H=-m kJ/mol
反应②:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)△H=-n kJ/mol
反应③:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0
根据上述的热化学方程式可以判断则2m_____n(填“大于”、“小于”、“等于”或“无法确定”)。
【答案】-93kJ/mol H2(g)+![]() O2(g)=H2O(l)△H -124.6kJ/mol 0.025mol·L-1·s-1 12.5% 10% 小于
O2(g)=H2O(l)△H -124.6kJ/mol 0.025mol·L-1·s-1 12.5% 10% 小于
【解析】
利用反应物键能之和减去生成物键能之和得到焓变值。利用盖斯定律计算焓变并完成热化学方程式的书写。利用“三段式”计算反应速率,转化率和体积分数。利用盖斯定律将①×2-②得到③式,再判断m和n值的相对大小,由此判断。
(1)反应:N2(g)+3H2(g)2NH3(g)△H,△H=反应物的键能之和-生成物的键能之和=945kJ/mol+3×436kJ/mol-6×391kJ/mol=-93kJ/mol;
(2)反应①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H= +49.0kJ/mol
反应②CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
已知水的气化热为44.0 kJ/mol,可以得到反应③H2O(g)=H2O(l)△H=-44kJ/mol
③×3+(②-①)得到3H2(g)+![]() O2(g)=3H2O(l)△H=-373.9kJ/mol,氢气燃烧热的热化学方程式H2(g)+
O2(g)=3H2O(l)△H=-373.9kJ/mol,氢气燃烧热的热化学方程式H2(g)+![]() O2(g)=H2O(l)△H =-124.6kJ/mol;
O2(g)=H2O(l)△H =-124.6kJ/mol;
(3)已知化学反应A(g)+B(g)C(g)+D(g),列出“三段式”,
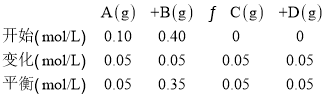
则A的平均反应速率v(A)=![]() ;
;
平衡时B的转化率为![]() ×100%=12.5%,C的体积百分数=C的物质的量分数=
×100%=12.5%,C的体积百分数=C的物质的量分数=![]() ×100%=10%;
×100%=10%;
(4)反应①:CO(g)+2H2(g)CH3OH(g)△H=-m kJ/mol
反应②:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)△H=- nkJ/mol
反应③:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0,
反应③=反应②-①×2,则-n-2(-m)<0,2m-n<0,则2m<n 。

【题目】(1)如图是部分元素原子的第一电离能I1随原子序数变化的曲线图(其中12号至17号元素的有关数据缺失)。
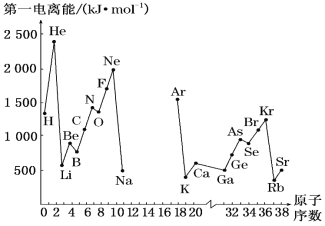
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围在哪两种元素之间为_____(填元素符号);
②图中第一电离能最小的元素在周期表中的位置是___________。
(2)已知元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出14种元素的电负性:
元素 | Al | B | Be | C | Cl | F | Li |
电负性 | 1.5 | 2.0 | 1.5 | 2.5 | 3.0 | 4.0 | 1.0 |
元素 | Mg | N | Na | O | P | S | Si |
电负性 | 3.0 | 0.9 | 3.5 | 2.1 | 2.5 | 1.8 |
已知:两成键元素间电负性差值大于1.7时,形成离子键,两成键元素间电负性差值小于1.7时,形成共价键。
①通过分析电负性值变化规律,确定Mg元素电负性值的最小范围________;
②判断下列物质是离子化合物还是共价化合物:
A.Li3N
Ⅰ.属于离子化合物的是_____;Ⅱ.属于共价化合物的是____;请设计一个实验方案证明上述所得到的结论____