题目内容
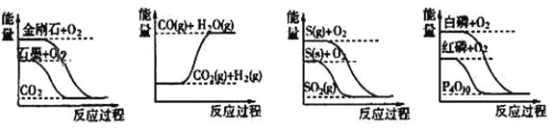
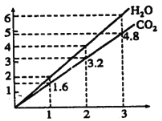
【题目】两种气态烃A,B组成的混合气体完全燃烧后得到CO2和H2O(g)的物质的量随混合烃的总物质的量的变化如图,则下列说法正确的是( )
A.混合烃中n(C):n(H) = 2:5B.混合烃中一定不含有乙烯
C.若混合烃为CH4、C4H4,则体积比为4:1D.若混合烃为CH4、C3H4,则体积比为3:7
【答案】AC
【解析】
从图中我们可以提取以下信息:当n(混)=2mol时,n(H2O)=4mol,n(CO2)=3.2mol,则平均组成为C1.6H4。
A.混合烃中n(C):n(H)=3.2mol:8mol = 2:5,A正确;
B.当n(混)=2mol时,n(H2O)=4mol,n(CO2)=3.2mol,则混合烃的平均组成为C1.6H4,则混合烃中必含有碳原子数大于1.6,氢原子数为4的有机物,其可能为乙烯,B不正确;
C.若混合烃为CH4、C4H4,体积比为4:1时,平均所含碳原子数为![]() =1.6,平均所含氢原子数为4,符合平均组成C1.6H4,,C正确;
=1.6,平均所含氢原子数为4,符合平均组成C1.6H4,,C正确;
D.若混合烃为CH4、C3H4,体积比为3:7,平均所含碳原子数为![]() =2.4,不符合平均组成关系,D不正确;
=2.4,不符合平均组成关系,D不正确;
故选AC。

 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案【题目】(1)从化学键的角度分析,化学反应的过程就是反应物的化学键被破坏和生成物的化学键的形成过程。已知反应:N2(g)+3H2(g)2NH3(g)△H。有关键能数据如下:
化学键 | H-H | N-H | N≡N |
键能)kJ/mol) | 436 | 391 | 945 |
根据表中所列键能数据可得△H=____________。
(2)已知:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H= +49.0kJ/mol
CH3OH(g)+![]() O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
O2(g)=CO2(g)+2H2O(g)△H= -192.9kJ/mol
已知水的气化热为44.0kJ/mol,表示氢气燃烧热的热化学方程式为______________。
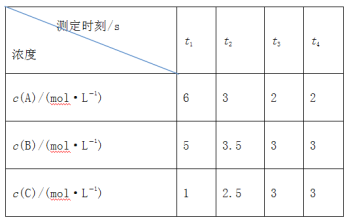
(3)已知化学反应A(g)+B(g)C(g)+D(g),900℃时向一个体积为2L的密闭容器中充入0.20mol A和0.80mol B,2s时达到平衡,A的浓度变化0.05mol/L,则A的平均反应速率v(A) =________,平衡时B的转化率为____ ,C的体积百分数为_______ 。
(4)CO、H2可用于合成甲醇和甲醚,其反应为(m、n均大于![]() ):
):
反应①:CO(g)+2H2(g)CH3OH(g)△H=-m kJ/mol
反应②:2CO(g)+4H2(g)CH3OCH3(g)+H2O(g)△H=-n kJ/mol
反应③:2CH3OH(g)CH3OCH3(g)+H2O(g)△H<0
根据上述的热化学方程式可以判断则2m_____n(填“大于”、“小于”、“等于”或“无法确定”)。