题目内容
【题目】瑞巴匹特为新型抗溃疡药,它可保护胃肠黏膜免受各种致溃疡因子的危害,其合成路线如图:
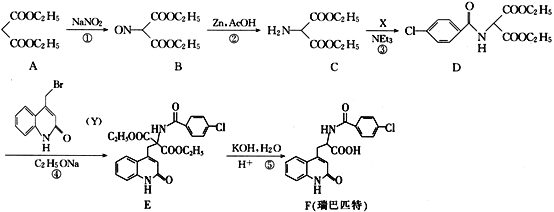
(1)A的化学名称为__,A与足量的NaOH溶液反应的化学方程式__。
(2)化合物D中含氧官能团的名称为__。
(3)反应①~④中,属于取代反应的是__(填序号)。
(4)C→D的转化中,生成的另一种产物为HCl,则X的结构简式为__。
(5)已知Y中的溴原子被-OH取代得到Z,写出同时满足下列条件的Z的一种同分异构体的结构简式:__。
Ⅰ.分子中含有一个苯环和一个五元环,且都是碳原子形成环;
Ⅱ.苯环上的一氯代物只有两种;
Ⅲ.能与NaHCO3溶液发生反应。
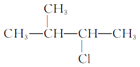
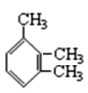
(6)已知:CH3CH2OH![]() CH3CH2Br,请写出以A和HOCH2CH2CH2OH为原料制备
CH3CH2Br,请写出以A和HOCH2CH2CH2OH为原料制备![]() 的合成路线流程图___(无机试剂任用)。
的合成路线流程图___(无机试剂任用)。
【答案】丙二酸二乙酯 C2H5OOCCH2COOC2H5+2NaOH![]() NaOOCCH2COONa+2C2H5OH 肽键、酯基 ①③④
NaOOCCH2COONa+2C2H5OH 肽键、酯基 ①③④ ![]()
![]() (或其它合理答案)
(或其它合理答案) 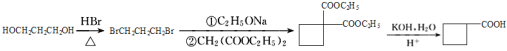
【解析】
分析瑞巴匹特合成路线:A与NaNO2反应,中间—CH2—的1个H被—NO取代得到B,B在Zn、AcOH作用下—NO被还原为—NH2得到C,C与X反应,C中—NH2上的1个H被![]() 取代得到D,反应④中D分子中与N相连的C上的H被
取代得到D,反应④中D分子中与N相连的C上的H被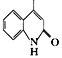 取代得到E,E经KOH、H2O处理后酸化得到目标产物F瑞巴匹特。可在此基础上解各小题。
取代得到E,E经KOH、H2O处理后酸化得到目标产物F瑞巴匹特。可在此基础上解各小题。
(1)A为丙二酸的二乙醇酯,化学名称为:丙二酸二乙酯;A为二元酯,与足量的NaOH溶液反应的化学方程式为:C2H5OOCCH2COOC2H5+2NaOH![]() NaOOCCH2COONa+2C2H5OH;
NaOOCCH2COONa+2C2H5OH;
答案为:丙二酸二乙酯;C2H5OOCCH2COOC2H5+2NaOH![]() NaOOCCH2COONa+2C2H5OH;
NaOOCCH2COONa+2C2H5OH;
(2)化合物D含氧官能团有![]() 、
、![]() ,名称分别为:肽键、酯基。
,名称分别为:肽键、酯基。
答案为:肽键、酯基;
(3)根据分析可知,反应①~④中,属于取代反应的是①:A分子中1个—CH2—的1个H被—NO取代,③:C中—NH2上的1个H被![]() 取代,④:D分子中与N相连的C上的H被
取代,④:D分子中与N相连的C上的H被 取代。
取代。
答案为:①③④;
(4)C→D的转化中,C与X反应,C中—NH2上的1个H被![]() 取代得到D,生成的另一种产物为HCl,则X为
取代得到D,生成的另一种产物为HCl,则X为![]() 和Cl相连的有机物,结构简式为
和Cl相连的有机物,结构简式为![]() 。
。
答案为:![]() ;
;
(5Y中的溴原子被-OH取代所得Z的结构简式为: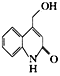 ,分子式为C10H9NO2。
,分子式为C10H9NO2。
由条件Ⅲ.能与NaHCO3溶液发生反应,可判断Z含1个-COOH;由条件Ⅰ.分子中含有一个苯环和一个五元环,且都是碳原子形成环,可判断Z可能有结构:![]() 或
或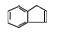 等;根据条件Ⅱ.苯环上的一氯代物只有两种,可判断苯环上应有2个取代基,一个为-COOH,另一个应为-NH2。据此可写出符合条件的Z的同分异构体为:
等;根据条件Ⅱ.苯环上的一氯代物只有两种,可判断苯环上应有2个取代基,一个为-COOH,另一个应为-NH2。据此可写出符合条件的Z的同分异构体为:![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等。
等。
答案为:![]() (或其它合理答案);
(或其它合理答案);
(6)参照瑞巴匹特合成路线中的步骤④、⑤,![]() 可由
可由![]() 经KOH、H2O处理后酸化而来,
经KOH、H2O处理后酸化而来,![]() 可由BrCH2CH2CH2Br与
可由BrCH2CH2CH2Br与![]() 发生取代反应而来,BrCH2CH2CH2Br可由HOCH2CH2CH2OH与HBr发生取代反应而来。所以,以A和HOCH2CH2CH2OH为原料制备
发生取代反应而来,BrCH2CH2CH2Br可由HOCH2CH2CH2OH与HBr发生取代反应而来。所以,以A和HOCH2CH2CH2OH为原料制备![]() 的合成路线流程图可设计为:
的合成路线流程图可设计为: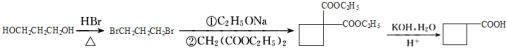 。
。
答案为: 。
。

 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案【题目】在工业废气和汽车尾气中含有多种氮氧化物,主要是NO 和NO2,都以NOx来表示。NOx能破坏臭氧层,产生光化学烟雾,是造成大气污染的主要来源之一。回答下列问题:
(1)已知 1mol 分子分解为单个原子所需要的能量为解离焓。 N2(g)、NO(g)、O2(g)的解离焓分别为941.7、631.8、493.7(单位kJ/mol),计算反应 2NO(g) = N2(g) + O2(g)的△H=_______kJ/mol,试判断NO(g)常温、常压下能否自发分解 ________填能或不能)。
(2)为防止光化学烟雾,除从工厂、汽车的设计进行改进外,也要采用某些化学方法。用焦炭还原NOx 的反应为2NOx(g) + xC(s)N2(g) + xCO2(g)
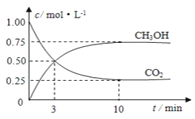
Ⅰ.在恒温条件下,2 molNO2(g)和足量 C(s)反应,测得平衡时 NO2(g)和 CO2(g)的物质的量浓度与平衡总压的关系如图所示:
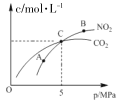
①A、B两点NO2平衡转化率的关系α(A)____α(B),平衡常数关系K(A)_____K(B)(填>、<或=)。
②计算C点时该反应的压强平衡常数Kp=_____MPa(Kp是用平衡分压代替平衡浓度)计算,分压=总压×物质的量分数)。
Ⅱ.现在向容积均为 2L 的两个密闭容器A、B中加入一定量的 NO(g)和足量的C(s),相同温度下测得两容器中n(NO)随时间变化情况如表所示:
0 | 20 | 40 | 60 | 80 | |
n(NO)/mol(A) | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
n(NO)/mol(B) | 1 | 0.8 | 0.65 | 0.53 | 0.45 |
B容器内反应在 100s时达到平衡状态,则0~100s内用 NO 表示的平均反应速率为v(NO)= ____________。
(3)近年来电化学方法在处理氮氧化物方面也起到了一定的作用,如图是一种氨气一二氧化氮燃料电池,常温下可将二氧化氮转化为氮气。
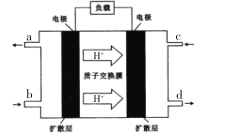
①c口通入的气体为______ ,写出负极反应的方程式 ________。
②若a、d口产生的气体体积共为1.568L(标况下),电路中通过的电子数为____。