题目内容
12. 某兴趣小组同学设计了如下装置(其中夹持仪器、加热仪器及冷却水管没有画出),用加热苯甲酸、浓H2SO4和乙醇混合物的方法来制备苯甲酸乙酯,并检验反应的部分副产物.且苯甲酸乙酯的沸点为213℃,乙醚的沸点为34.6℃.
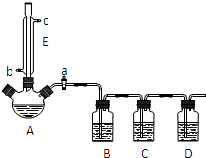
某兴趣小组同学设计了如下装置(其中夹持仪器、加热仪器及冷却水管没有画出),用加热苯甲酸、浓H2SO4和乙醇混合物的方法来制备苯甲酸乙酯,并检验反应的部分副产物.且苯甲酸乙酯的沸点为213℃,乙醚的沸点为34.6℃.(1)关闭活塞a、接通竖直冷凝管的冷凝水,给A加热30分钟,制备.仪器E的作用是冷凝回流(或导气兼冷凝).
(2)上述反应的副产物可能有:乙醚(CH3CH2-O-CH2CH3)、乙烯、SO2、水等.
①打开活塞a,在竖直冷凝管上方塞上塞子,通过B、C、D装置检验SO2和乙烯.已知C中盛放的试剂是NaOH溶液,B、D中应盛放的试剂依次分别是品红、溴水(或酸性KMnO4溶液或溴的CCl4溶液).
②有同学拟通过红外光谱仪鉴定所得产物中是否含有“-CH2CH3”,来确定副产物中存在乙醚.请你对该同学的观点进行评价:不可以,产物苯甲酸乙酯也含有“-CH2CH3”.
(3)通过下列实验方案,可以提纯苯甲酸乙酯.
①为除去产品中杂质,先将三口烧瓶中残液倒入盛有冷水的烧杯中,并加入饱和Na2CO3溶液.
②用分液法可分离上述有机层和水层,分液完成后,取出有机层的操作是将有机层从上口倒入一个干燥的锥形瓶中.
③向锥形瓶中加入适量豆粒大小的无水氯化钙干燥剂,至醚层澄清透明;过滤得醚层,然后将醚层加入到干燥的蒸馏烧瓶中蒸馏,蒸馏过程中控制的温度为34.6℃.
分析 (1)有机物苯甲酸、乙醇易挥发,仪器E起冷凝回流作用;
(2)①B装置检验二氧化硫的存在,C装置除去二氧化硫防止干扰乙烯的检验;D装置检验乙烯;
②根据红外光谱仪的作用,进行分子结构和化学组成分析;苯甲酸乙酯和乙醚都含有乙基“-CH2CH3”;
(3)①饱和Na2CO3溶液可溶解乙醇,中和酸,从而除去产品中的杂质;
②有机层的密度小于水,在上层,应从分液漏斗上口倒入干燥锥形瓶中,再进行干燥;
③依据物质沸点不同,通过控制温度蒸馏得到乙醚和酯,乙醚易挥发,说明乙醚沸点较低,苯甲酸乙酯沸点高于乙醚,蒸馏过程中控制的温度为乙醚的沸点.
解答 解:(1)有机物苯甲酸、乙醇易挥发,仪器E为冷凝管起冷凝回流作用,充分利用原料,
故答案为:冷凝回流(或导气兼冷凝);
(2)①打开活塞a,在竖直冷凝管上方塞上塞子,通过B、C、D装置检验SO2和乙烯.二氧化硫具有漂白性,通过品红能使品红褪色验证二氧化硫的存在,C中盛放的试剂是NaOH溶液,二氧化硫能和氢氧化钠溶液反应而被吸收,反应为:SO2+2NaOH=Na2SO3+H2O,防止干扰乙烯的检验,D装置用溴水(或溴的CCl4溶液);CH2=CH2+Br2→CH2BrCH2Br,溴水褪色,或酸性KMnO4溶液,乙烯被氧化高锰酸钾溶液褪色,
故答案为:品红、溴水(或酸性KMnO4溶液或溴的CCl4溶液);
②红外光谱仪利用物质对不同波长的红外辐射的吸收特性,进行分子结构和化学组成分析,产物苯甲酸乙酯( )、也含有-CH2CH3,所以不能通过红外光谱仪来确定副产物中是否存在乙醚(CH3CH2-O-CH2CH3),
)、也含有-CH2CH3,所以不能通过红外光谱仪来确定副产物中是否存在乙醚(CH3CH2-O-CH2CH3),
故答案为:不可以,产物苯甲酸乙酯也含有“-CH2CH3”;
(3)①得到酯中含有挥发出的苯甲酸、乙醇,饱和Na2CO3溶液可溶解乙醇,中和酸,从而除去产品中的杂质,
故答案为:饱和Na2CO3溶液;
②有机层的密度小于水,在上层,分液完成后,有机层从分液漏斗上口倒入一个干燥的锥形瓶中,再进行干燥,
故答案为:将有机层从上口倒入一个干燥的锥形瓶中;
③提纯苯甲酸乙酯:向锥形瓶中加入适量豆粒大小的无水氯化钙干燥剂,至醚层澄清透明;过滤得醚层,然后将醚层加入到干燥的蒸馏烧瓶中蒸馏,苯甲酸乙酯的沸点为213℃,乙醚的沸点为34.6℃,苯甲酸乙酯沸点高于乙醚,需蒸馏出杂质乙醚,所以蒸馏过程中控制的温度为乙醚的沸点34.6℃,
故答案为:34.6℃.
点评 本题主要考查了苯甲酸乙酯的制取实验,产物的检验实验操作步骤和过程分析判断、物质的分离与提纯等,明确反应原理、掌握实验基本操作和有机物性质是解题关键,题目难度中等.

 某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.
某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.Ⅰ.配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g.
(2)从表中选择称量NaOH固体所需要的仪器是(填字母):a b e.
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 |  |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
(1)写出该反应的热化学方程式(中和热为57.3kJ/mol):$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-57.3kJ/mol.
(2)取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①请填写下表中的空白:
| 温度 实验 次数 | 起始温度t1/℃ | 终止温度 t2/℃ | 温度差平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 31.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度.
| A. | 溴乙烷$\stackrel{NaOH/水}{→}$乙醇$\stackrel{浓硫酸}{→}$乙烯$\stackrel{Br_{2}}{→}$1,2-二溴乙烷 | |
| B. | 溴乙烷$\stackrel{Br_{2}}{→}$1,2-二溴乙烷 | |
| C. | 溴乙烷$\stackrel{氢氧化钠/醇}{→}$乙烯$\stackrel{HBr}{→}$溴乙烷$\stackrel{Br_{2}}{→}$1,2-二溴乙烷 | |
| D. | 溴乙烷$\stackrel{氢氧化钠/醇}{→}$乙烯$\stackrel{Br_{2}}{→}$1,2-二溴乙烷 |
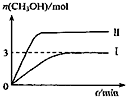
| A. | 曲线Ⅱ对应的条件改变是减小压强 | |
| B. | 若T2℃时,上述反应平衡常数为0.42,则T2<T1 | |
| C. | 在T1℃时,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和 5 mol H2O(g),则达平衡前v(正)>v(逆) | |
| D. | 在T1℃时,若起始时向容器中充入4.5molCO2、6mol H2,平衡时容器内压强P=$\frac{{P}_{1}}{2}$ |
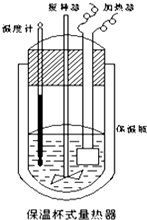 在如图所示的量热计中,将100mL0.50mol•L CH3COOH溶液 与100mL0.55mol•L-1NaOH溶液混合.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,溶液的密度均近似为1g•mL-1.实验中某同学计算中和热,记录数据如下:
在如图所示的量热计中,将100mL0.50mol•L CH3COOH溶液 与100mL0.55mol•L-1NaOH溶液混合.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,溶液的密度均近似为1g•mL-1.实验中某同学计算中和热,记录数据如下:| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 醋酸溶液 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 25.0 | 25.1 | 27.8 |
| 2 | 25.1 | 25.3 | 27.9 |
| 3 | 25.2 | 25.5 | 28.0 |
(2)CH3COOH的中和热的文献值为56.1KJ•mol-1,则请你分析在(1)中测得的实验值偏差可能的原因①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等.
(3)实验中NaOH过量的目的是使碱稍稍过量,为了能保证CH3COOH溶液完全被中和,从而提高实验的准确度.
(4)CH3COOH的中和热与盐酸的中和热绝对值相比,HCl的较大,原因是CH3COOH是弱酸,只是少部分电离,CH3COOH发生电离时要吸热.

 二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2).以下是氯气与硫合成二氯化硫的实验装置.
二氯化硫(SCl2)熔点-78℃,沸点59℃,密度1.638g/mL,遇水易分解,二氯化硫与三氧化硫作用可生成重要化工试剂亚硫酰氯(SOCl2).以下是氯气与硫合成二氯化硫的实验装置. ,由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为SCl2+SO3=SOCl2+SO2.
,由二氯化硫与SO3作用生成亚硫酰氯的化学方程式为SCl2+SO3=SOCl2+SO2.