题目内容
【题目】化合物E(结构简式为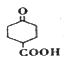 )是合成消毒剂α——萜品醇(结构简式为
)是合成消毒剂α——萜品醇(结构简式为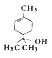 )的中间体。由甲苯经一系列变化制取E的流程如下:
)的中间体。由甲苯经一系列变化制取E的流程如下:
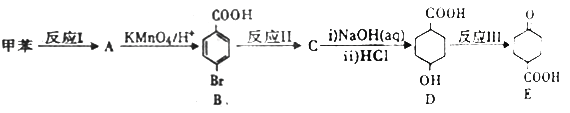
请回答下列问题:
(1)化合物E中含有的官能团名称为________,α—萜品醇的分子式为_________,甲苯的结构简式为_____。
(2)反应I的化学方程式为____________。
(3)反应II的反应类型是__________________。
(4)反应III的试剂与条件为__________________。
(5)写出一种符合下列条件的有机物的结构简式_____________。
①是化合物D的一种同分异构体;②能与NaHCO3反应;③能与新制氢氧化铜浊液在加热条件下反应生成红色固体;④在核磁共振氢谱上有5个峰。
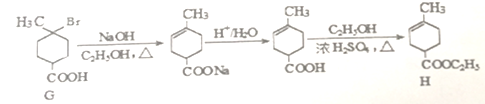
(6)下面是由化合物E合成一种α—萜品醇的流程的一部分,请将其中有G生成H的几步流程补充完整(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件).________________。
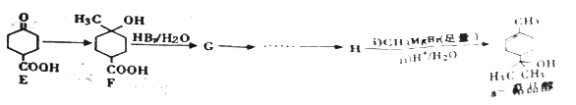
提示: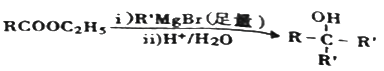
【答案】 羰基、羧基 C10H18O ![]()
![]() 加成反应(或还原反应) O2、Cu或Ag,
加成反应(或还原反应) O2、Cu或Ag, 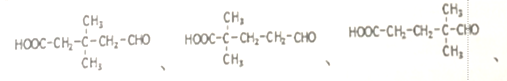
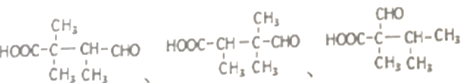
【解析】![]() 反应1是与Br2发生取代反应得到A为
反应1是与Br2发生取代反应得到A为![]() ,氧化后得到
,氧化后得到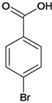 经与H2加成得到C
经与H2加成得到C![]() ,碱性条件下水解后再酸化得到D,再去氢氧化得到E。
,碱性条件下水解后再酸化得到D,再去氢氧化得到E。
(1)化合物E(结构简式为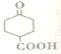 )含有的官能团名称为羰基、羧基,α—萜品醇的分子式为C10H18O,甲苯的结构简式为
)含有的官能团名称为羰基、羧基,α—萜品醇的分子式为C10H18O,甲苯的结构简式为![]() ,(2)反应I的化学方程式为
,(2)反应I的化学方程式为![]() ;(3)反应II的反应类型是加成反应(或还原反应)(4)反应III是去氢氧化,反应III的试剂与条件为O2、Cu或Ag, ;(5)写出一种符合下列条件的有机物的结构简式①是化合物D的一种同分异构体;分子式为C7H12O3,②能与NaHCO3反应;说明含有-COOH,③能与新制氢氧化铜浊液在加热条件下反应生成红色固体;说明含有醛基,④在核磁共振氢谱上有5个峰。故满足条件的物质有
;(3)反应II的反应类型是加成反应(或还原反应)(4)反应III是去氢氧化,反应III的试剂与条件为O2、Cu或Ag, ;(5)写出一种符合下列条件的有机物的结构简式①是化合物D的一种同分异构体;分子式为C7H12O3,②能与NaHCO3反应;说明含有-COOH,③能与新制氢氧化铜浊液在加热条件下反应生成红色固体;说明含有醛基,④在核磁共振氢谱上有5个峰。故满足条件的物质有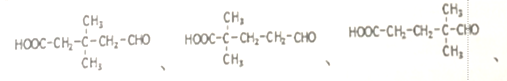
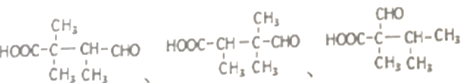
(6)从F到G是醇的卤代反应,G在碱的醇溶液中发生消去反应,得到含双键的盐,酸化后生成酸,在浓硫酸作用下得到酯,流程如下: