题目内容
【题目】在某一容积为2 L的密闭容器中,加入0.8 mol的H2和0.6 mol 的I2,在一定的条件下发生如下反应:H2(g)+I2(g) ![]() 2HI(g) ΔH<0反应中各物质的浓度随时间变化情况如图:
2HI(g) ΔH<0反应中各物质的浓度随时间变化情况如图:
(1)根据如图数据,反应开始至达到平衡时,平均速率v(HI)为________。

(2)反应达到平衡后,第8 min时:①若升高温度,化学平衡常数K________(填“增大”、“减小”或“不变”),HI浓度的变化正确的是________(用如图中a~c的编号回答)。

②若加入I2,H2浓度的变化正确的是________(用如图中d~f的编号回答)。
(3)反应达到平衡后,第8 min时,若反应容器的容积扩大一倍,请在图中画出8 min后HI浓度的变化情况。
 ______
______
【答案】0.167 mol/(L·min) 减小 c f 
【解析】
根据v=△c/△t,计算平均速率v(HI);
(2)升高温度,平衡逆向移动,生成物浓度减少;
(3)若加入I2,平衡正向移动,H2浓度减少;
(4)反应是体积不变的反应,改变压强平衡不移动,容器的容积扩大一倍,平衡物质浓度减小.
(1)平均速率v(HI)=(0.5mol/L-0)÷3min=0.167molL-1min-1,故答案为:0.167molL-1min
(2)①该反应放热,升高温度,平衡逆向移动,生成物浓度减少,化学平衡常数减小,故答案为:减小,c;
②若加入I2,平衡正向移动,H2浓度减少,故答案为:f;
(3)H2(g)+I2(g)2HI(g),反应是体积不变的反应,改变压强平衡不移动,容器的容积扩大一倍,平衡时物质浓度减小,碘化氢浓度减小一半为0.25mol/L,画出的变化图象如图: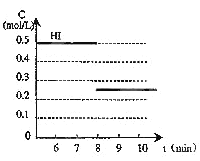 ,故答案为:
,故答案为:

【题目】在当今社会,氮的氢化物和氧化物与我们的生活息息相关.
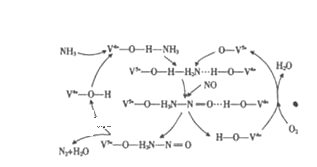
(1)NO是一种污染物,工业上用NH3、O2脱除烟气中NO的原理如图所示,该原理中NO最终转化为______(填化学式),V4+﹣O﹣H在反应过程中作___________。当消耗2molNH3和0.5molO2时,除去的NO在标准状况下的体积为____________L。
(2)N2H4是发射航天火箭的常用燃料,已知:N2H4(g)+O2(g)=N2(g)+2H2O(g) △H=﹣538kJ·mol﹣1。断开1mol下列化学键系数的能量分别为N﹣H:390kJ、N≡N:946kJ、O﹣H:460kJ、O=O:498kJ。则断开1molN﹣N需要吸收的能量是__________.
(3)工业制硝酸时,会发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) △H<0。
4NO(g)+6H2O(g) △H<0。
①若其它条件不变,则下列图象不正确的是_____(填字母)。
A. B.
B.  C.
C. D.
D.
②在1L容积固定的密闭容器中充入NH3和O2发生该反应,部分物质的浓度随时间的变化如下表所示。
| c(NH3)/mol·L﹣1 | c(O2)/mol·L﹣1 | c(NO)mol·L﹣1 |
0 | 1.2 | 1.75 | 0 |
4min | 0.4 | 0.75 | 0.8 |
6min | 0.4 | 0.75 | 0.8 |
8min | 0.6 | 1 | 0.6 |
9min | 0.6 | 1 | 0.6 |
10min | 1.05 | 1 | 1.05 |
12min | … | … | … |
0~4min内,用O2表示该反应的平均反应速率为______mol·L﹣1·min﹣1。反应6~8min时改变了反应条件,改变的反应条件可能是___________。
【题目】在一定温度下,将气体 X 和气体 Y 各 0.16mol 充入 ![]() 恒容密闭容器中,发生反应:
恒容密闭容器中,发生反应:![]()
![]() ,一段时间后达到平衡。反应过程中测定的数据如下表:
,一段时间后达到平衡。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
下列说法正确的是
A.反应前 ![]() 的平均速率
的平均速率 ![]()
B.该温度下此反应的平衡常数 ![]()
C.其他条件不变,再充入 ![]() Z ,平衡时 X 的体积分数不变
Z ,平衡时 X 的体积分数不变
D.其他条件不变,降低温度,反应达到新平衡前 v(逆)> v(正)