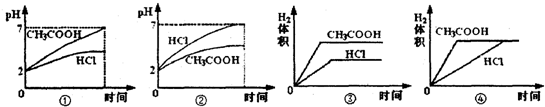
题目内容
常温下,有四种溶液:
回答下列问题:
(1)①与③等体积混合,则溶液pH______7(填“>”或“=”或“<”等,下同).
(2)①稀释到原来的10倍后的溶液pH______④溶液的pH.
(3)④和⑤两溶液中水电离出的c(H+):④______⑤.
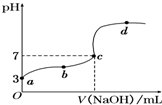
(4)①与③混合,若溶液pH=7,则两溶液体积关系为V(NaOH)______V(CH3COOH).
(5)②与④等体积混合,则溶液pH______7,其所得溶液中的溶质组成可能为:______.
| ① | ② | ③ | ④ | ⑤ |
| 0.0001mol?L-1 CH3COOH溶液 | pH=10 NaOH溶液 | 0.0001mol?L-1 NaOH溶液 | pH=4 CH3COOH溶液 | pH=4 NH4Cl溶液 |
(1)①与③等体积混合,则溶液pH______7(填“>”或“=”或“<”等,下同).
(2)①稀释到原来的10倍后的溶液pH______④溶液的pH.
(3)④和⑤两溶液中水电离出的c(H+):④______⑤.
(4)①与③混合,若溶液pH=7,则两溶液体积关系为V(NaOH)______V(CH3COOH).
(5)②与④等体积混合,则溶液pH______7,其所得溶液中的溶质组成可能为:______.
(1)①与③等体积混合,恰好生成醋酸钠,为强碱弱酸盐,溶液显碱性,所以pH>7,故答案为:>;
(2)①的浓度为0.0001mol/L,pH=4的CH3COOH溶液的浓度大于0.0001mol/L,稀释到原来的10倍,④的氢离子浓度大,浓度越大,pH越小,所以稀释后的pH为①>④,
故答案为:>;
(3)④为酸,溶液中c(H+)=0.0001mol/L,则由水电离的c(H+)=10-10mol/L,⑤为能水解的盐,促进水的电离,所以水电离出的c(H+)=0.0001mol/L,所以由水电离的c(H+)为④<⑤,故答案为:<;
(4)①与③混合,若溶液pH=7,结合(1)可知,醋酸应过量,即醋酸的体积大于碱的体积,故答案为:<;
(5)②与④等体积混合,得到醋酸和醋酸钠的混合溶液,醋酸的电离大于盐的水解,溶液显酸性,故答案为:<;CH3COONa和CH3COOH.
(2)①的浓度为0.0001mol/L,pH=4的CH3COOH溶液的浓度大于0.0001mol/L,稀释到原来的10倍,④的氢离子浓度大,浓度越大,pH越小,所以稀释后的pH为①>④,
故答案为:>;
(3)④为酸,溶液中c(H+)=0.0001mol/L,则由水电离的c(H+)=10-10mol/L,⑤为能水解的盐,促进水的电离,所以水电离出的c(H+)=0.0001mol/L,所以由水电离的c(H+)为④<⑤,故答案为:<;
(4)①与③混合,若溶液pH=7,结合(1)可知,醋酸应过量,即醋酸的体积大于碱的体积,故答案为:<;
(5)②与④等体积混合,得到醋酸和醋酸钠的混合溶液,醋酸的电离大于盐的水解,溶液显酸性,故答案为:<;CH3COONa和CH3COOH.

练习册系列答案
相关题目