题目内容
【题目】有机物![]() 同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只2种;③
同时满足下列条件:①含苯环且不含甲基;②苯环上一氯取代物只2种;③![]() 与足量的
与足量的![]() 反应生成
反应生成![]() ;④遇
;④遇![]() 溶液不显色.A如图所示转化关系:
溶液不显色.A如图所示转化关系:
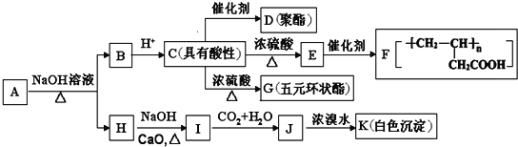
已知:![]()
回答下列问题:
(1)E中官能团名称_____,H的分子式为_______.
(2)由C生成G的反应类型是________.
(3)A的结构简式为____,G的结构简式为_________.
(4)①写出CD反应的化学方程式_________;
②写出I→J反应的离子方程式_____________.
(5)C的同分异构体中能同时满足下列条件:a.能发生银镜反应,b.能发生皂化反应;c.能与![]() 反应产生
反应产生![]() ,共有_____种(不含立体异构).其中核磁共振氡谱显示为3组峰,且峰面积比为6:1:1的是_________(写结构简式).
,共有_____种(不含立体异构).其中核磁共振氡谱显示为3组峰,且峰面积比为6:1:1的是_________(写结构简式).
【答案】碳碳双键和羧基 ![]() 酯化反应
酯化反应 ![]()
![]()
![]()
![]() +CO2+H2O
+CO2+H2O ![]() +HCO
+HCO![]() 5
5 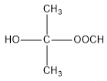
【解析】
A在碱性条件下水解得到B与H,A中含有酯基,B酸化得到C具有酸性,则C中含有羧基,C反应可以得到聚酯,则C中还含有羟基,由F的结构逆推可知E为CH2=CHCH2COOH,C发生消去反应得到E,E发生加聚反应生成F,C在浓硫酸作用下得到五元环状酯G,则C为HOCH2CH2CH2COOH,G为![]() ,B为HOCH2CH2CH2COONa,C发生缩聚反应得到D为
,B为HOCH2CH2CH2COONa,C发生缩聚反应得到D为![]() 。结合A分子式,H中含7个碳原子,H发生信息中脱羧反应得到I,I与二氧化碳、水作用得到J,J与浓溴水作用生成白色沉淀K,则J中含有酚羟基,1mol A与足量的NaHCO3反应生成1mol CO2,说明A分子中含有1个-COOH,而A遇FeCl3溶液不显色,则A不含酚羟基,则A中酯基为羧酸与酚形成的,A中含苯环且不含甲基,且苯环上一氯取代物只有2种,则A中含有2个对位位置的取代基,可推知A的结构简式为:
。结合A分子式,H中含7个碳原子,H发生信息中脱羧反应得到I,I与二氧化碳、水作用得到J,J与浓溴水作用生成白色沉淀K,则J中含有酚羟基,1mol A与足量的NaHCO3反应生成1mol CO2,说明A分子中含有1个-COOH,而A遇FeCl3溶液不显色,则A不含酚羟基,则A中酯基为羧酸与酚形成的,A中含苯环且不含甲基,且苯环上一氯取代物只有2种,则A中含有2个对位位置的取代基,可推知A的结构简式为:![]() ,H为
,H为![]() ,I为
,I为![]() ,J为
,J为![]() ,K为
,K为 。
。
(1)E为CH2=CHCH2COOH,E中官能团名称碳碳双键和羧基,H为![]() ,H的分子式为
,H的分子式为![]() ;故答案为:碳碳双键和羧基;
;故答案为:碳碳双键和羧基;![]() ;
;
(2)C为HOCH2CH2CH2COOH,C在浓硫酸作用下得到五元环状酯G,G为,由C生成G的反应类型是酯化反应;故答案为:酯化反应;
(3)由A的结构简式为![]() ,G的结构简式为
,G的结构简式为![]() ;故答案为:
;故答案为:![]() ;
;![]() ;
;
(4)①C发生缩聚反应得到D为![]() ,CD反应的化学方程式
,CD反应的化学方程式![]() ;故答案为:
;故答案为:![]() ;
;
②I![]() 与二氧化碳、水作用得到J,I→J反应的离子方程式
与二氧化碳、水作用得到J,I→J反应的离子方程式![]() +CO2+H2O
+CO2+H2O ![]() +HCO
+HCO![]() ;故答案为:
;故答案为:![]() +CO2+H2O
+CO2+H2O ![]() +HCO
+HCO![]() ;
;
(5)C为HOCH2CH2CH2COOH,C的同分异构体中能同时满足下列条件:a.能发生银镜反应,说明含有醛基,b.能发生皂化反应,含有甲酸形成的酯基,c.能与Na反应产生H2,还含有羟基,可以看作丙烷中H原子被-OH、-OOCH取代,-OOCH取代甲基中H原子,-OH有3种位置,-OOCH取代亚甲基中H原子,-OH有2种位置,共有5种(不含立体异构),其中核磁共振氢谱显示为3组峰,且峰面积比为6﹕1﹕1的是: (写结构简式);故答案为:5;
(写结构简式);故答案为:5; 。
。

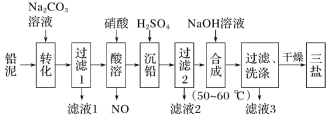
【题目】直接排放含SO2的烟气会形成酸雨危害环境。利用钠碱循环法可脱除烟气中的SO2。
(1)用化学方程式表示SO2形成硫酸型酸雨的反应原理为__。
(2)在钠碱循环法中,Na2SO3溶液作为吸收液,可由NaOH溶液吸收SO2制得,该反应的离子方程式为__。
(3)吸收液吸收SO2的过程中,pH随n(![]() ):n(
):n(![]() )变化关系如表:
)变化关系如表:
n( | 91:9 | 1:1 | 1:91 |
pH | 8.2 | 7.2 | 6.2 |
①上表判断NaHSO3溶液显性__(填“酸”或“碱”),用化学平衡原理解释__。
②当吸收液呈中性时,溶液中离子浓度关系正确的是(填字母编号)__。
a.c(Na+)=2c(![]() )+c(
)+c(![]() )
)
b.c(Na+)>c(![]() )>c(
)>c(![]() )>c(H+)=c(OH-)
)>c(H+)=c(OH-)
c.c(Na+)+c(H+)=c(![]() )+c(
)+c(![]() )+c(OH-)
)+c(OH-)
(4)当吸收液的pH降至约为6时,送至电解槽再生。再生示意图如下:
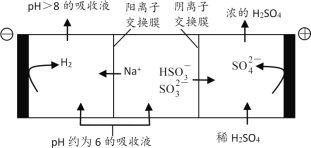
①![]() 在阳极放电的电极反应式是__。
在阳极放电的电极反应式是__。
②当阴极室中溶液pH升至8以上时,吸收液再生并循环利用。简述再生原理__。
【题目】已知某溶液X可能由K+、Mg2+、Cu2+、Ag+、Ba2+、Al3+、Fe2+、![]() 、
、![]() 、
、![]() 、I-、
、I-、![]() 、
、![]() 中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
中的若干种离子组成。某化学兴趣小组通过下列实验确定了其组成。
(1)根据下列实验步骤和现象,推断实验结论:
实验步骤与实验现象 | 实验结论 |
Ⅰ.观察溶液:无色透明 | ①原溶液中一定不含的离子是____。 |
Ⅱ.取适量该溶液,加入过量的硝酸,有气体生成,并得到无色溶液 | ②原溶液中一定不含的离子是_____,一定含有的离子是____。 |
Ⅲ.在Ⅱ所得溶液中再加入过量的碳酸氢铵溶液,有气体生成,同时析出白色沉淀A | ③原溶液中还一定含有的离子是____,生成沉淀A的离子方程式为____。 |
Ⅳ.在Ⅲ所得溶液中再逐滴加入氢氧化钡溶液至过量,加热也有气体生成,同时析出白色沉淀B | ④白色沉淀B中一定含有___,可能含有____。 |
(2)上述实验步骤Ⅳ中开始阶段一定发生的离子方程式是______。
(3)该化学兴趣小组的同学为了进一步确定B的成分,取一定量经洗涤后的B与Y溶液反应,白色固体的物质的量与Y溶液体积之间的关系如图所示。
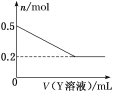
Y可能为(填化学式)____,B的组成为______。
【题目】(1)为了检验和除去下表中的各种杂质(括号里的为杂质),请从①中选出适当的检验试剂,从②中选出适当的除杂试剂,将所选的答案用字母填入相应的空格内。
物质 | 检验试剂 | 除杂试剂 |
(Ⅰ)甲烷(乙烯) | ________。 | ________。 |
(Ⅱ)酒精(水) | ________。 | ________。 |
①检验试剂:
A.无水硫酸铜 B.酸性高锰酸钾溶液
C.水 D.氢氧化钠溶液
②除杂试剂:
a.无水硫酸铜 b.乙酸
c.新制的生石灰 d.溴水
除杂时,乙烯发生反应的化学方程式为____________________。
(2)如图,在左试管中先加入2 mL 95%的乙醇,并在摇动下缓缓加入3 mL浓硫酸,再加入2 mL乙酸,充分摇匀。按图连接好装置,用酒精灯对左试管小火加热3~5 min后,改用大火加热,当观察到右试管中有明显现象时停止实验。
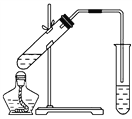
试回答:
在右试管中通常加入________溶液,实验生成的乙酸乙酯,其密度比水________,是有特殊香味的液体。分离右试管中所得乙酸乙酯的操作为(只填名称)________。反应中加入浓硫酸的作用是_____________________________________________________。